二価の弱毒化生インフルエンザウイルスワクチンは、ブタの漂流した H1N2 および H3N2 臨床分離株を防御します パート 2
Aug 02, 2023
2.5. 酵素免疫測定法 (ELISA)
コーティング抗原を作成するために、SD435 および SD467 を MDCK 細胞内で増殖させ、ショ糖勾配超遠心分離を使用して精製しました。 ウイルスの不活化は、97 パーセントのプロピオラクトンを 1:1000 (v/v) の濃度でウイルスに添加することによって起こりました (Thermo Fisher Scientific、AAB2319703)。 この混合物を 4 °C で一晩振盪し、β-プロピオラクトンの加水分解を促進するために 37 °C で 2 時間インキュベートし、使用するまで -80 °C で保管しました。
抗原と免疫は切っても切れない関係にあります。 抗原とは、細菌、ウイルス、腫瘍細胞など、免疫系によって認識され、免疫反応を引き起こすあらゆる物質を指します。一方、免疫とは、これらの抗原に応答する体の能力を指します。
抗原と免疫の関係は、簡単な比喩で説明できます。運動には十分なトレーニングと栄養補給が必要であるのと同じように、免疫の向上も、抗原と、対応する免疫細胞および免疫分子との繰り返しの接触に依存します。 生産する。 免疫系が抗原に遭遇すると、再感染から私たちを守るための記憶細胞とともに、特定の抗体または免疫細胞を生成して攻撃します。
科学は、良い生活習慣と食習慣を身につけることが免疫力の向上に役立つことを証明しています。 例えば、清潔を保つ、禁煙、適度な運動、睡眠習慣などは細菌やウイルスなどの抗原の侵入を減らすのに役立ちます。 同時に、野菜や果物、全粒穀物、魚など、抗酸化物質、ビタミン、ミネラルが豊富な食品を食べることも免疫力の向上に役立ちます。
つまり、抗原と免疫の関係は非常に密接です。 抗原との繰り返しの接触と適切な生活習慣によってのみ免疫力は継続的に向上し、さまざまな病気を予防し、治療することができます。 したがって、私たちは前向きな姿勢を維持し、病気から身を守るために良い生活習慣を身につけるべきです。 免疫力を向上させる必要があることがわかります。 シスタンケには、ビタミンCやカロテノイドなどのさまざまな抗酸化物質が豊富に含まれているため、免疫力の向上に役立ちます。これらの成分はフリーラジカルを除去し、酸化ストレスを軽減し、免疫系の抵抗力を改善します。

カンクサ・デザートティコーラサプリメントをクリックしてください
ワクチン接種および攻撃によって誘導されるswIAV特異的IgGレベルを測定するために、1回目(20日目)および2回目(30日目)のワクチン接種後、および剖検(36日目)前にブタ血清を採取した。
精製プロピオラクトン不活化ウイルス SD435 (1 μg/mL) および SD467 (2 μg/mL) を炭酸塩/重炭酸塩コーティング緩衝液 (pH 9.6) で希釈し、1{{ 12}}0 μL/ウェル (Thermo Labsystems、オタワ、オンタリオ州、カナダ、3655) を加え、4 °C で一晩インキュベートしました。 一晩インキュベートした後、コーティングしたプレートを TBST (0.1 M Tris、0.17 M NaCl、および 0.05 パーセント Tween 20) で 4 回洗浄し、それに血清または BALF の 4 倍段階希釈物を添加しました。プレートを 2 枚ずつプレートに移し、室温で 2 時間インキュベートします。 血清を1:10の開始希釈で添加し、BALFを希釈せずに添加した。 以前に定義された陽性対照血清と、以前の研究でワクチン接種を受けていないブタから採取した適切な陰性対照、血清、および BALF のサンプルを各プレートで実行しました [14]。
プレートをTBSTで4回洗浄した後、ヤギ抗ブタIgG(HプラスL)ホスファターゼ標識アフィニティー精製抗体(1:5000)(Sigma Aldrich、SAB3700435)またはマウス抗ブタIgA(Serotec、MCA658)で洗浄しました( TBSTで希釈した1:300)を添加し、室温で1時間インキュベートした。 IgA ELISA は、ビオチン化ヤギ抗マウス IgG (H プラス L) 抗体 (CALTAG、バーリンゲーム、カリフォルニア州、米国、M30015) とストレプトアビジンアルカリホスファターゼ溶液 (Jackson ImmunoResearch、ペンシルバニア州ウェストグローブ) を両方とも 1 時間添加して開発しました。室温で。
インキュベーション後、IgG プレートと IgA プレートの両方を TBST で 4 回洗浄し、p-ニトロフェニルリン酸基質 (PNPP) [10 mg/mL p-ニトロフェニルリン酸二(トリス) 塩結晶 (Sigma-Aldrich) 、1パーセントのジエタノールアミン(Sigma−Aldrich)、0.5mg/mLのMgCl2、およびpH9.8](1mg/mL)を添加し、室温で2時間インキュベートした。
0.3 M エチレンジアミン四酢酸 (EDTA) を添加して反応を停止し、分光光度計でプレートを 490 nm を基準として 405 nm で読み取った。 サンプルの力価は、そのサンプルのODが規定のカットオフ(既知の陰性サンプルの平均ODに標準偏差の2倍を加えたもの)より高くなる最高希釈として定義されました。
2.6. ウイルス中和 (VN) アッセイ
MDCK 細胞 (3.5 × 104 個) を 96- ウェルプレートに播種しました。 血清と BALF を 56 °C で 30 分間加熱不活化しました。 2 倍希釈の血清と BALF を 4 つずつプレートに加え、60 μL の希釈血清または BALF を、100 TCID50 を含む等量の SD435 または SD456 と 37 °C で 1 時間インキュベートしました。 次に、混合物 100 μL を MDCK 細胞に添加し、感染後 48 時間および 72 時間 (pi) で細胞病原性効果 (CPE) を記録しました。 中和抗体力価は、4 つのウェルのうち少なくとも 2 つで細胞を CPE から完全に保護する各血清サンプルの最高希釈率でした。

2.7. ウイルスの判定
収集後、肺サンプルはすぐに氷上に置かれ、処理するまで -80 °C で凍結されました。 処理のために、各肺組織の重量を量り、1×抗生物質抗真菌剤 (Thermo Fisher Scientific、15240-062) を補充した 10 パーセント (w/v) 濃度の MEM を添加しました。 肺組織を TissueLyser II (Qiagen、ヒルデン、ドイツ) で 30 Hz で 5 分間ホモジナイズし、続いて 4 ℃、5000 x g で 10 分間遠心分離しました。 均質化された上清を収集し、さらなる分析まで -80 °C で保存しました。 鼻腔スワブを 15 秒間ボルテックスし、4 ℃、1600 x g で 25 分間遠心分離しました。 上清を収集し、さらなる分析まで -80 °C で保存しました。 ウイルス力価は、肺については TCID50 アッセイによって、鼻腔スワブについては定量的 RT-PCR によって決定されました。
2.8. RNA 抽出と定量 RT-PCR (qRT-PCR)
攻撃後の鼻腔スワブ中の SD467 および SD435 のウイルス RNA レベルを決定するために、qRT-PCR を実施しました。 標準曲線は、力価が既知の SD435 および SD467 から抽出した RNA を使用して作成しました。 簡単に説明すると、RNeasy Plus Mini Kit (Qiagen、トロント、オンタリオ州、カナダ、74136) を使用して、200 μL の鼻洗浄液から vRNA を抽出しました。 RNA は、ユニバーサル インフルエンザ プライマー Uni12 および SuperScript III Transcriptase (Invitrogen、バーリントン、オンタリオ州、カナダ) を使用して cDNA に変換されました [19]。 qPCR は、Power SYBR Green PCR Master Mix (Applied Biosystems)、5 μL cDNA、および 1 μL の 10 μM フォワードおよびリバース プライマーを使用して、StepOnePlusTM リアルタイム PCR システム (Applied Biosystems、カリフォルニア州、米国) で 3 回実行しました。 PCR 反応は、アニーリング温度 58 °C で 40 サイクル実行されました。 qPCR プライマーのすべての配列は、ご要望に応じて入手可能です。
2.9. 統計分析
統計分析は、GraphPad Prism 8 ソフトウェアを使用して実行されました。 Mann-Whitney 検定と Kruskal-Wallis ノンパラメトリック検定が使用されました。 有意差は * (p < 0.05)、** (p < 0.01)、*** (p < 0.001) で示されます。 、または **** (p < 0.0001)。 ns=は重要ではありません。
3. 結果
3.1. 二価ワクチンのワクチン接種により新たな臨床分離株に対する防御が得られる
これらの新しい臨床分離株に対する二価ワクチンによる防御を評価するために、攻撃ウイルスに対する物理的反応と気道内でのウイルス複製を測定しました。 すべてのグループにおいて、ウイルス感染後 5 日間、体温を毎日記録しました。 模擬ワクチン接種を受け、SD435 (H3N2) (MEM/SD435) または SD467 (H1N2) (MEM/SD467) でチャレンジされたブタは、ウイルスチャレンジ後 1 日目に典型的な体温上昇を示し、体温の中央値は 40.6 °C と 41.1 °C でした。それぞれC。 このスパイクは、SD435 (二価/SD435) または SD467 (二価/SD467) で攻撃されたワクチン接種グループでは見られず、中央値温度はそれぞれ 39.4 °C と 39.6 °C でした。 攻撃後 2 ~ 5 日目の体温は、ワクチン接種群と非ワクチン接種群の両方で約 39 °C でした (図 2A)。
攻撃から5日後、すべてのブタを剖検し、肺を完全に摘出し、存在する病変の量を定量化するために分析した。 二価/SD435 グループは最小限の病変を示したか、まったく病変を示さず、全肺病変の中央値は 0.65% でした。 MEM/SD435 グループは、ワクチン接種したグループよりも病変が有意に多く、中央値は 5.1% (p= 0.0025) でした (図 2B)。 二価/SD467 グループでは、7 頭中 5 頭の豚に少量の病変がありました (<2%), one had minor lesions (3.75%), and one outlier had high lesions (31%), with a group median of 1.9%. Compared with the vaccinated group, the MEM/SD467 group had a higher degree of lesions with a median of 4.55% (p = 0.0417) (Figure 1C).

肺では、二価/SD435 グループと二価/SD467 グループの両方のウイルス力価が低く、平均はそれぞれ 8.6 PFU/mL/gr と 3.0 PFU/mL/gr でした。 逆に、MEM/SD435 グループと MEM/SD467 グループはウイルス量が多く、平均はそれぞれ 656.1 と 9118.2 PFU/mL/gr でした (両方とも p=0.0025) (図 3A、 B)。 同様の傾向が鼻腔スワブでも見られました。 二価/SD435 グループでは、チャレンジ後 1、3、5 日目 (dpc) では鼻の力価が低かったのに対し、MEM/SD435 グループでは力価がわずかに上昇し、日が進むにつれて (ns) 増加しました (図 3C)。 二価/SD467 グループでは、鼻の力価も低く、チャレンジ後 1 日目と 5 日目では平均 5 PFU/mL 未満、3 日目では 10.0 PFU/mL でした。 力価は毎日 MEM/SD467 グループで高く、1 日あたり平均 4123.6 PFU/mL/gr (p=0.0278)、1 日あたり 77233.1 PFU/mL/gr (p=0.0009) でした。 3dpc、および 5dpc (ns) で 65.2 PFU/mL/gr (図 3D)。

全体として、これらの結果は、二価ワクチンが攻撃株に対してかなりの程度の防御を提供し、肺および鼻腔におけるこれら 2 つの swIAV 分離株の感染に関連する肺病変とウイルス複製を減少させたことを示唆しています。
3.2. 二価ワクチンはチャレンジ株に対する免疫反応を誘導します
二価ワクチンによるプライムブーストワクチン接種後の、両方の攻撃株に対する血清および肺特異的な抗体反応を測定しました。 最初のワクチン接種後 (2 日目 0) と 2 回目のワクチン接種後 (30 日目) にブタから血清を採取しました。 チャレンジウイルス SD435 (H3N2) および SD467 (H1N2) を捕捉抗原として使用し、血清中のウイルス特異的 IgG 抗体応答を測定しました。 SD435では、最初のワクチン接種(20日目)後、MEMと二価ワクチン接種グループの抗体力価の間に有意差はありませんでした。 しかし、SD467に対する抗体力価は20日目にワクチン接種群で有意に高かった(p= 0.0321)。 2回目のワクチン接種後(31日目)、SD435およびSD467の両方に対する抗体力価は、MEMモックワクチン群よりもワクチン接種群の方が有意に高かった(p<0.0001)(図4A、B)。 具体的には、捕捉抗原 SD435 に対する、MEM 模擬ワクチン接種グループの血清 IgG 力価は 20 日目と 30 日目で平均 52 でしたが、二価ワクチングループでは 311 (20 日目) と 4852 (30 日目) でした (図 3A)。 SD467 に対する、模擬ワクチン接種 MEM グループの血清 IgG 力価は 39 (20 日目) および 38 (30 日目) でしたが、二価ワクチングループでは 219 (20 日目) および 3509 (30 日目) でした (図 3B)。

2 つの攻撃株に対する血清中の中和抗体力価を測定したときにも、同様の傾向が見られました。 繰り返しますが、ワクチンの1回投与後(2日目0)のSD435に対するMEMグループと二価ワクチン接種グループの中和抗体力価の間に有意差はありませんでした(図5A、B)。 SD467 に対して、抗体レベルは 1 回ワクチン後 2 日目0に有意に高かった(p=0.0069)。 両方のウイルスに対して、2 価ワクチン群では 2 回目の投与後 30 日目に抗体力価の増加が見られました (p < 0.0001)。 MEM 模擬ワクチン接種グループの力価は SD435 でチャレンジされ、平均 1 (20 日目) および 3 (30 日目) でしたが、二価グループの力価は平均 10 (da20) および 77 (30 日目) でした (図 5A)。 SD467 でチャレンジした MEM 模擬ワクチン接種グループの力価は平均 0 (20 日目) および 2 (30 日目) でしたが、二価ワクチングループの力価は平均 10 (20 日目) および 54 (30 日目) でした (図 5B)。

剖検時(36日目)、肺内の抗体レベルを測定できるように、各ブタからBALFを収集した。 攻撃ウイルス SD435 および SD467 を捕捉抗原として使用して、ウイルス特異的 IgA および IgG 応答を測定しました。 SD435 に対して、MEM 模擬ワクチン群の IgA レベルは平均 17 でしたが、二価ワクチン群の力価は平均 95 で有意に高かった (p=0.0014) (図6A)。 SD467 では、IgA レベルは模擬ワクチン群では平均 18 でしたが、二価ワクチン群では 158 と有意に高かった (p= 0.0185) (図 6B)。 IgG に関しては、MEM モックワクチン群の SD435 に対する力価は平均 3 でしたが、二価ワクチン群では平均 138 と有意に高かった (p < 0.0001) (図 6C)。 SD467 に対する IgG 抗体は、MEM モックワクチングループでは平均 16 でしたが、二価ワクチングループでは平均 259 と有意に高かった (p < 0.0001) (図 6D)。
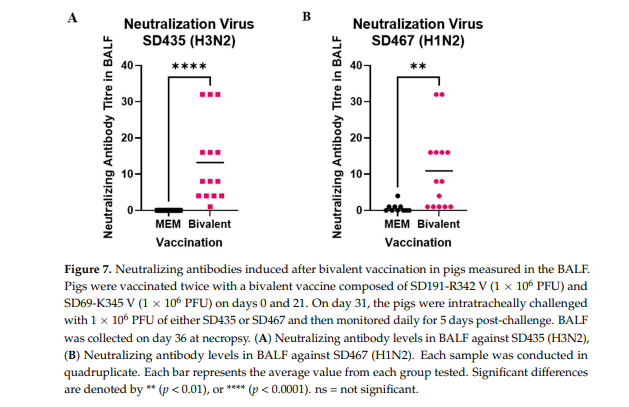
BALF の中和抗体に関しては、傾向は IgA および IgG ELISA で見られたものと同様でした。 SD435 に対する中和抗体力価は、MEM モックワクチングループでは検出できませんでしたが、二価ワクチングループでは平均 13.2 と有意に高かった (p < 0.0001) (図 7A)。 同様に、SD467 に特異的な抗体力価は、MEM モックワクチングループでは平均 0.7 でしたが、二価ワクチングループでは平均力価が 10.9 と有意に高かった (p= 0.0002) (図 7B)。 まとめると、このデータは、二価ワクチンの 2 回の投与が、これら 2 つの非相同臨床分離株に対して、強力な全身性体液性反応と肺における局所免疫反応を誘発することを示しています。

4。討議
我々は以前、エラスターゼ依存性ウイルス SD191-R342V および SD69.K345V がブタにおいて完全に弱毒化され非毒性であること、およびこの二価 LAlV による 2 回のワクチン接種が強力な免疫応答を誘発し、相同な SD191 による感染に対する防御を提供することを実証しました( H1N2) および SD69 (H3N2) 株 [14)。 この現在の研究では、抗原ドリフトを起こした最近の臨床分離株に対して二価ワクチンが生体内で耐えられるかどうかをテストしたいと考えました。 SD467 は、SD191 と同様、カナダで出現した Ho-3 抗原グループのメンバーですが、主要な抗原部位に多数の変異を獲得しています (12,15]。同様に、SD435 は H3N2 IV-E クラスターを表します)これはカナダ西部に存在し、重要な H3 抗原部位に SD69 に存在するものからの複数のアミノ酸置換を持っています (17]。

二価LALVは、SD435(H3N2)またはSD467(H1N2)のいずれかで攻撃した場合、ワクチン接種されたブタの病変を有意に減少させ、攻撃1日後にMEM(模擬)ワクチン接種群で見られた体温の急上昇を防止した。 また、肺における両株のウイルス複製の減少と、鼻腔スワブにおける SD467 (H1N2) の減少にもつながりました。 興味深いことに、SD435 (H3N2) の鼻力価は、同一のサンプリング方法にもかかわらず、ワクチン接種群と非ワクチン接種群の両方で低く、この株が鼻腔に対してそれほど指向性を持たない可能性があることを示唆しています。 肺病変スコアが 31 と高い、グループ内の外れ値のブタに関しては、体温測定では攻撃時のスパイクは示されず、肺内のウイルス力価は 10 PFU/g/mL 未満でした。 血清中の抗体レベルと局所的な肺反応も、ワクチン接種を受けた他のすべての豚と同じでした。 このことから、病変はインフルエンザに関連したものではなかったと推測されます。 血清分析により、ワクチンを2回投与した後に両株に対して強い免疫反応が生じたことが明らかになり、肺の局所分析でも同じことが判明した。 抗体指向性の表面糖タンパク質は、IAV 感染に対する防御において最も重要であるため、ワクチン接種されたブタに見られる高レベルの中和抗体および IgG および IgA は、生体内で見られる防御をサポートします [20]。
全不活化ウイルス (WIV) ワクチンは、アジュバントを使用して古典的に製剤化された豚に最も一般的に利用可能であり、流行している株との再集合のリスクがないため、安全なアプローチであると考えられています。 しかし、それらはミスマッチ株に対しては効果が限られており、ミスマッチ株に対して使用するとワクチン関連増強呼吸器障害(VAERD)を引き起こすことが示されています。 それらの有効性は、母親由来抗体 (MDA) の存在下でも低下します [4]。 北米で市販されているものには、H1N1、H1N2、および H3N2 クラスター IV-A および IV-B を含む 4 価の製剤として米国で入手可能な FluSure XP® が含まれます [21]。 Flusure XP® の古い製剤は、2000 年から 2005 年の間に分離された 2 つの H1N1 株と 1 つの H1N2 株を含むカナダで入手可能です [22]。 北米両国では、H1N1pdm09 株で構成される一価ワクチンである FluSure® Pandemic と、H1N1、H1N2、および H3N2 を含む Pneumostar SIV Complete (米国ノースカロライナ州グリーンズボロの Elanco Inc.) が入手可能です。 H1N1 および H3N2 サブタイプ株を含むニューモスター SIV (GOC、USDA) [23、24]。 これらの市販ワクチンは、北米の豚インフルエンザワクチンの約 50% を占め、ワクチン接種の残りの 50% は自家ワクチンです [4]。
代替ワクチンプラットフォームに関しては、組換えアルファウイルス由来レプリコン粒子ワクチンが米国で認可されました[4]。 このワクチンプラットフォームは、ゲノムが変更されたアルファウイルスを採用しており、ウイルスの構造遺伝子が選択された遺伝子に置き換えられ、アルファウイルスの複製が欠損します。 この RNA は自己複製するため、ワクチン プラットフォームは目的の遺伝子の高発現をもたらし、インフルエンザの場合、HA と核タンパク質 (NP) の両方が抗原として検査されています [25]。 研究では、このプラットフォームの使用により、抗原的に HA が一致する攻撃および HA が一致しない攻撃、ならびに NP が一致しない株から保護されることが示されていますが、このプラットフォームは MDA の存在から保護することはできませんでした。
豚インフルエンザに対する最初の LAIV は、2017 年に米国農務省 (USDA) によって承認されました。Ingelvac Provenza™ は、米国で分離された 2 つの株の HA と NA を TX98 バックボーンで発現させた二価 H3N2 および H1N1 ワクチンです。非構造タンパク質 (NS1) の切断によって減弱される [14,26]。 LAIV は自然感染を模倣し、鼻腔内に送達されると上気道の粘膜免疫の増加につながります。 不活化ワクチンが主に全身性 IgG 抗体の産生を引き起こすのに対し、弱毒化生ワクチンは気道で粘膜 IgA を誘導する可能性があり、また、より多くの T を含む内部インフルエンザタンパク質への免疫系の曝露による細胞媒介性反応の増加も引き起こす可能性があります。細胞エピトープ[27]。 これにより、不一致株に対する保護が強化されます。
これらは、MDA の存在下で部分的な保護を示しています。 完全な IgG 抗体は下気道でより蔓延しており、ポリマー IgA 抗体はブタの上気道で優勢であり、ほとんどの場合二量体として存在します [28]。 これらの抗体は局所的に産生され、プロテアーゼによる分解に抵抗する分泌成分の助けを受けて上皮細胞層を通って輸送され、そこで粘膜に残ります[28、29]。 IgA 抗体は、入ってくる病原体に対する適応免疫系の防御の第一線であり、シアル酸受容体へのウイルスの付着をブロックするように機能します [30]。 ポリマー IgA 抗体は、おそらく多価結合のため、モノマー IgG 抗体よりも広範囲に交差反応性があります [31]。 研究では、これらの抗体は、豚血清に含まれる IgG または単量体 IgA よりも感染細胞から新たに形成される IAV の放出をはるかに効率的に防止できることも示されており、IgA のポリマー構造がウイルス子孫の架橋に有利であることが示唆されています。感染細胞表面に発現する HA に影響を与える [31-33]。 したがって、局所的な IgA 抗体応答は IAV 感染に対する防御に不可欠であり、ヒトにおける防御と相関関係があることが示唆されています [34]。
ただし、LAIV のリスクは、循環株との再集合の可能性です。 米国での系統学的研究では、Ingelvac Provenza™ に含まれるワクチン株と再集合した新しい株が流通していることが判明しました [26]。 エラスターゼ依存性 LAIV プラットフォームは、このリスクを軽減します。これは、エラスターゼタンパク質がブタの気道に非常に不足しているため、ワクチンウイルスの複製が非常に制限され、再集合が起こる時間枠も非常に限られているためです。 今後の研究には、この二価ワクチンの再集合リスクの評価や、このワクチンがMDAの存在下でどのように耐えられるかが含まれる予定です。 これは LAIV の大きな利点の 1 つであるため、このワクチンの細胞媒介応答をテストすることも興味深いでしょう。 結論として、二価エラスターゼ依存性LAIVは、カナダ西部で見つかった新たな臨床分離株にも保護を拡大し、豚インフルエンザワクチン市場のいくつかのギャップを埋めることになるだろう。
著者の寄稿:
概念化、YZ; 方法論、YZ、LA。 正式な分析、ロサンゼルス。 捜査、LAとUB-C。 リソース、SD; 執筆—初稿準備、ロサンゼルス。 執筆 - レビューと編集、YZ、UB-C.、SD。 監修、YZ; 資金調達、YZ すべての著者は原稿の出版版を読み、同意しました。
資金提供:
この研究は、サスカチュワン州農業省の農業開発基金(ADF)から資金提供を受けました。 LA は、サスカチュワン大学公衆衛生学部のワクチン学および免疫療法 (V&I) 奨学金によって部分的に支援されています。 VIDO は、イノベーション サスカチュワン州および農業省を通じてサスカチュワン州政府から、メジャー サイエンス イニシアチブを通じてカナダ イノベーション財団から CL3 施設 (InterVac) の運営資金を受けています。
治験審査委員会の声明:
適用できない。

データの可用性に関する声明:
この研究のデータと分析はすべてこの記事で報告されています。
謝辞:
動物実験のためにすべての動物実験を行ってくださった VIDO の獣医師と動物技術者に感謝いたします。 この作品は、VIDO ディレクターの許可を得て、原稿シリーズ #1005 として公開されます。
利益相反:
著者は利益相反がないことを宣言します。
参考文献
ウェブスター、RG インフルエンザウイルス:種間の伝播と次の人類パンデミックの出現との関連性。 アーチ。 ヴィロル。 補足 1997、13、105–113。 [パブメッド]
2. リー、Y。 Robertson, I. 豚インフルエンザの疫学。 アニム。 ディス。 2021 年 1 月 21 日。 [CrossRef] [PubMed]
3. Donovan, T. 豚の成長におけるインフルエンザの役割。 ミネソタ大学: 米国ミネソタ州ミネアポリス、2005 年。
4. グラシア、JCM; ピアース、DS; マジック、A. Balasch, M. 豚におけるインフルエンザ A ウイルス: 疫学、課題、ワクチン接種戦略。 正面。 獣医-科学。 2020、7、647。 [CrossRef] [PubMed]
5. Ma, W. 豚インフルエンザウイルス: 現状と課題。 ウイルス研究所 2020、288、198118。[相互参照]
6. 鈴木裕也; 伊藤哲也; 鈴木哲也; オランダ、RE; チェンバース、TM; 木曽真。 石田博史; Kawaoka, Y. インフルエンザ A ウイルスの宿主範囲の決定因子としてのシアル酸種。 J.Virol. 2000、74、11825–11831。 [相互参照]
7. サン、H. シャオ、Y. リュー、J. 王D. リー、F。 ワン、C. リー、C. 朱、J. ソング、J. サン、H. 他。 ヒトへの感染を促進する 2009 年パンデミック ウイルス遺伝子を持つ、ユーラシアで蔓延している鳥様 H1N1 豚インフルエンザ ウイルス。 手順 国立 アカド。 科学。 米国 2020、117、17204–17210。 [相互参照]
8. ヘンリッツィ、D. ペトリック、PP; ニューサウスウェールズ州ルイス。 グラーフ、A. ペシア、A. スターリック、E. ブライトハウプト、A. ストレベロー、G. ルッターマン、C. パーカー、LMK。 他。 ヨーロッパの家畜豚個体群の監視により、潜在的に人獣共通感染症である可能性のある豚インフルエンザ A ウイルスの新たな保有源が特定されました。 細胞宿主微生物 2020、28、614–627.e6。 [相互参照]
9. アラバマ州ヴィンセント。 マ、W。 ケンタッキー州ラガー。 バージニア州ジャンケ。 JA、リヒト 豚インフルエンザウイルス:北米の視点。 上級 ウイルス研究所 2008、72、127–154。
10. ラジャオ、DS; アンダーソン、TK; キティクーン、P. ストラットン、J. ニューサウスウェールズ州ルイス。 アラバマ州ヴィンセント 米国における現代豚 H1 インフルエンザウイルスの抗原性および遺伝的進化。 ウイルス学 2018、518、45–54。 [相互参照]
11. メナ、I. I ネルソン、M. ケザダ・モンロイ、F. ダッタ、J. コルテス・フェルナンデス、R. ララ・プエンテ、JH; カストロペラルタ、F. LF、クーニャ。 トロヴァン、ニューサウスウェールズ州。 ロザノ=デュベルナール、B. 他。 2009 年メキシコの豚における H1N1 インフルエンザのパンデミックの起源。 Elife 2016、5、e16777。 [相互参照]
12. ミシガン州ネルソン。 カルヘイン氏、MR。 トロヴァン、ニューサウスウェールズ州。 パトナヤック、DP。 ハルピン、RA; リン、X。 シルツ、MH。 ダス、SR; Detmer、SE カナダと米国におけるブタにおけるインフルエンザ A (H1) ウイルスの出現と進化。 J. ヴィロル将軍。 2017、98、2663–2675。 [相互参照] [PubMed]
13. チャウハン、RP; Gordon, ML 世界中の豚集団におけるインフルエンザウイルスの蔓延と循環を分析する系統的レビュー。 病原体 2020、9、355。 [CrossRef]
14. ランドレス、S. デトマー、S. ゲルツ、V. Zhou, Y. 二価の弱毒生インフルエンザ ウイルス ワクチンは、ブタの H1N2 および H3N2 ウイルス感染を防ぎます。 獣医。 微生物。 2020、253、108968。[CrossRef] [PubMed]
15. マコーミック、K. ジャン、Z。 朱、L. サウスカロライナ州ローソン。 ランゲンホルスト、R. ランズバーグ、R. ブルーニック、C. トレイシー、MC。 ハーティグ、HR; マビー、LM; 他。 遺伝的に異なるインフルエンザA H1N1サブタイプウイルスに由来するキメラヘマグルチニン遺伝子を含む組換えインフルエンザAウイルスの構築および免疫原性の評価。 PLoS ONE 2015、10、e0127649。 [相互参照] [PubMed]
For more information:1950477648nn@gmail.com
