結果
フェニルエタノイド配糖体とイリドイドの質量断片化の法則
フェニルエタノイド配糖体は CD の主な化学成分です。 イソアクテオシド、シスタノシド F、テーブルサイド A、エキナコシド、アクテオシド、2'-アクチルラクテオシドの標準溶液を取得し、異なるレベルの衝突エネルギーを与えて (表 1)、対応する MS2 マップを取得しました (図 1)。 。

詳細については:
david.deng@wecistanche.com WhatApp:86 13632399501
質量分析分析により、フェニルエタノイド配糖体は同様の質量スペクトル断片化パターンを有し、マイナスイオンモードでの切断経路には主に (1) エステル結合切断: 中性カフェオイル基 (C9H3O6、162.03) と中性アセチル基 (C2H2O、C2H2O、162.03) の喪失が含まれることが明らかになりました。 42.00); (2) グリコシド切断: 中性ラムノース残基 (C6H10O4、146.05) および中性グルコース残基 (C6H10O5、162.05) の損失。 高分解能質量分析により、カフェオイル (162.03) とグルコース残基 (162.05) を区別することができました。

イリドイド アジュゴール、カタルポール、テニポシド酸、ゲニポシド、および8-エピデオキシロガン酸標準溶液を採取し、さまざまな衝突エネルギーを与えて、対応する MS2 マップを取得しました (図 2)。
イリドイドグリコシドは同様の質量スペクトル断片化パターンを持ち、マイナスイオンモードでの切断経路には主に次のものが含まれます。(1) グリコシド切断: 中性グルコース残基 (C6H10O5、162.05) の損失。 (2) 中性 CO2 (43.99) および H2O (18.01) の損失。

CD、CD‑NP、CD‑HP 抽出物中の化合物の同定
UPLC‑QTOF‑MSE 分析
クロマトグラフィー条件の最適化を実施しました。 次に、Cistanche Herba の化合物を、高い CE と低い CE を備えた陰イオン モードと陽イオン モードの両方で評価しました。 得られた結果は、これらの化合物については、ネガティブ モードの適合性がポジティブ モードと比較して高いことを明らかにしました。 図 3 は、番号付きピークで追跡された MS ベーシック ピーク イオン (BPI) クロマトグラムを示しています。 UPLC-Q-TOF-MSE 分析で検出された各イオンの強度は、m/z 値、正規化されたピーク面積、および保持時間で構成されるデータ マトリックスを生成するために、全イオン数に関して正規化されました。
UNIFI プラットフォーム上での CD およびその加工製品のコンポーネントの評価
CD およびその処理生成物から -SEM (n=6) モードを使用して、フェニルエタノイド配糖体 (PhG)、イリドイド、リグナン、オリゴ糖を含む合計 97 の化合物が同定されました (表 2)。 したがって、95、91、および 94 の成分が CD、CD-NP、および CD-HP で検出されました。 このうち、64 種類がフェニルエタノイド、13 種類がイリドイド、その他 20 種類の化合物が測定されました。 CDとその加工品の化学組成は類似しているが、その成分量が異なることが判明した。

加工品の化学成分のばらつき
多変量データ行列の分析には、Simca-P 13.0 ソフトウェアを使用しました。 PCA の前には、すべての変数が平均中心化およびパレートスケール化され、その後、潜在的な判別変数が特定されました。 PCA スコア プロットでは、すべての点が個々のサンプルを示しました。 化学成分が類似しているサンプルは隣接して分散され、成分が異なるサンプルは分割されました。 PCA (図 4) で見られるように、CD-HP のグループは CD および CD-NP のグループから分離されました。

To distinguish CD from CD-HP and CD-NP, OPLS-DA, permutation test, S-plot, and VIP value were developed. (Figs. 5, 6, 7) The obtained results revealed that many components were key characteristic components of each product. The screening condition was the VIP>1とP<0.05. From the date of the S-plot, the characteristic components evaluated, which were commonly existing in the three groups were.
図 8 から、4'-O-カフェオイル基を有するアクテオシド (54)、シスタノシド C (74)、カンネオシド II (43)、オスマンチュシド (75)、および 2'-アクチルラクテオシド (80) の強度がわかりました。 8-O- -d-グルコピラノシル部分 (図 9 を参照) は、米ワインで処理した後に減少しましたが、イソアセトシド (60)、イソシスタノシド (71)、イソカンネオシド I (69) の強度は減少しました。 、6'-O-カフェオイル基を有するイソマルチノシド(86)(図9参照)が、特にCD-NP基で増加しました。 イソアクテオシドと同じ 6'-O-カフェオイル基を有するタフなチューブロシド B (72) は、その 2'-アセチル基により強度が低下しました。 6'-O- -d-グルコピラノシル部分基を有するエキナコシド (38) とシスタノシド B の強度は増加しましたが、チューブロシド A (55) の強度は 2'-アセチル基のため減少しました。

私たちの研究チームは、アクテオシドとイソアクテオシドの熱安定性も研究し、アクテオシドは水、メタノール、黄酒溶液中で不安定であり、加熱条件下で部分的にイソアクテオシドに変換できることを発見しました。 しかし、イソアクテオシドの熱安定性は、特に黄酒溶液中では優れていました。 図 10 は、処理中に CD 内の PhG が変化する可能性を示しています。
ラットの代謝産物の同定
高分解能質量分析データから、代謝産物とプロト分子化合物の正確な分子量と元素組成が分析され、比較されました。 TCM の同じ種類の化合物は代謝修飾において類似性を示したので、in vitro での植物化学成分の相関関係は in vivo での代謝産物にまで及ぶ可能性があります。 一方、従来の生体内変換経路に基づいて、分子量の合理的な変化が推測されました。 最後に、代謝産物の MSE 質量スペクトルと質量スペクトルにおけるプロト化合物の断片化経路を分析することにより、代謝産物を同定しました [21、22]。 ブランクサンプルと比較して、クロマトグラム質量スペクトル、代謝反応の可能性、化合物構造の特徴、および質量スペクトルの断片化規則によって提供される情報に基づいて、その成分が生体内で同定されました。 表 3 を参照してください。

フェニルエタノイド配糖体関連代謝産物の同定
処理にはUNIFIプラットフォームを使用しました。 図 11 は、CD およびその処理製品の尿、糞便、血漿の TIC クロマトグラフを示しています。 ブランクサンプルと比較して、ラットでは 10 種類のプロトタイプ成分と 44 種類の代謝物を含む合計 54 種類の代謝物が同定され、そのうち 24 種類、49 種類、6 種類が糞便、尿、血漿中に含まれていました。
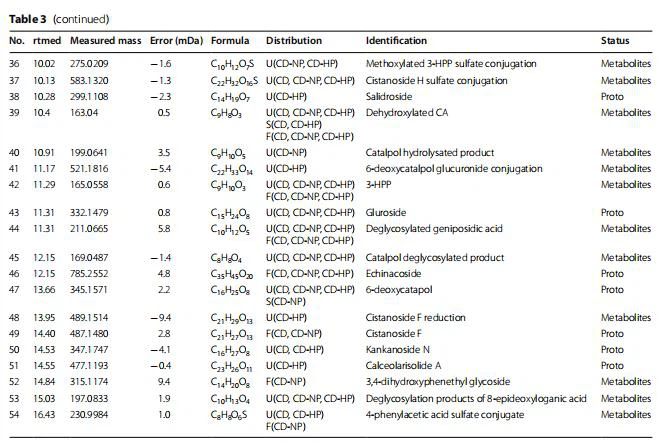
正確な質量、断片化カスケード、生体内変換による予測可能な中性損失に基づいて、合計 35 個のフェニルエタノイド配糖体関連代謝産物が暫定的に評価されました。 フェニルエタノイド配糖体の関連代謝物は、典型的なカフェオイル フラグメント m/z 461.1605 のように、同様の質量スペクトルのフラグメンテーション パターンを持ち、その後、生体内でグリコシド結合とエステル結合によってさらに加水分解され、ヒドロキシチロソール (HT) (m/ z 153.0504、C8H10O3、4.73分)およびカフェ酸(CA)(m/z 179.0389、C9H7O4、0.77分)、図12Aを参照。
M11 は、式 C8H10O3 で m/z 153.0504 で [M-H]- を示し、HT として識別されました。 M16 は m/z 329.0851 で [M-H]- を示し、これは HT よりも 176 Da 高く、これが HT のグルクロン酸抱合代謝産物である可能性があることを明らかにしました。 M26 の [M-H]- は m/z 343.1037 で、HT-グルクロニドより 14 Da 高かった。 したがって、M26 は HT メチル化グルクロニドであると同定されました。 M17 は、m/z 233.0112、HT より 80 Da の [M-H]- に基づいて HT 硫酸塩として同定され、さらにメチル化される可能性があり、その後 M22 が生成され、m/z 247.0278 を示しました。 HT メチル化硫酸化代謝物。 M7(m/z 167.0335)およびM5(m/z 167.0762)は、それぞれ酸化生成物およびメチル化HTであると考えられた(図12B)。

M1 は m/z 179.0389 で [M-H]- を示し、解明された分子式は C9H7O4 であり、カフェ酸 (CA) として同定されました。 M25 は m/z 355.0704 で [M-H]- を示し、これは CA よりも 176 Da 高く、CA のグルクロン酸抱合代謝物である可能性があることを示しました。 M27はm/z 258.994でCAより80Da高かったため、硫酸CAとして解明し、M35(m/z 273.0064)を生成することができました。 M4 は m/z 193.0524 で [M-H]- を与え、CA より 14 Da 高いため、CA メチル化代謝物として同定されました。 M39 は m/z 163.04 の CA 脱ヒドロキシル化代謝産物であり、硫酸化されて M32 (m/z 242.9951) になる可能性があります。
M33 (m/z 181.0491、C9H10O4、9.06 分) は CA の還元生成物、つまり 3,4- ジヒドロキシ ベンゼン プロピオン酸であり、メチル化されて M19 (m/z 195.0623、C10H12O4、0.93分)。 M33 は脱水されて M43、つまり 3-HPP (m/z 165.0558、C9H10O3、11.29 分)、M31 (m/z 341.0942、C15H17O9、8.90 分)、および M29 (m/z 245.0125、C9H10O6S、 8.52分)はグルクロン酸抱合および硫酸化生成物であった(図12C)。
フェニルエタノイドグリコシド関連代謝産物の場合、重要な代謝カスケードは第 II 相代謝反応、すなわちグルクロン酸抱合、メチル化、および硫酸化でした。 提案されているフェニルエタノイドの代謝カスケードを図 13 に示します。

イリドイド関連代謝産物の同定
代謝産物の元素組成、MSE 断片化、および関連文献を分析することにより、合計 19 個のイリドイド関連代謝産物が暫定的に特定されました。
評価されました。 イリドイドグリコシドはグリコシド結合によって加水分解されて、対応するアグリコンを形成しました。 M8のTe m/z 185.117は、グルコース残基の損失によって得られたアジュゴールよりも162Da小さい。 M40 (m/z 199.0641、Rt 10.91 分) は、カタルポールの脱グリコシル化生成物でした。 M45 m/z 169.0487、Rt 12.15分)は、カタルポール脱グリコシル化代謝物のそれより30Da未満であり、CH2O代謝物の分子の除去として同定された。 M34 (m/z 151.0352、Rt 9.08 分) は、H2O 代謝産物のさらなる損失でした。
M44 (m/z 211.0665、Rt 11.31 min) はゲニポシドの脱グリコシル化代謝産物であり、M37 (m/z 197.0833、Rt 15.03 min) は 8- エピデオキシロガン酸の脱グリコシル化でした。 イリドイドの代謝反応は、脱グリコシル化の第I相代謝として明らかにすることができた(図12D)。
CD とその加工製品間の血漿、尿、糞便中の代謝プロファイリングの比較
血漿中の 2 つのプロトタイプ、尿中の 7 つ、および糞便中の 3 つのプロトタイプを比較しました。 CD には 7 つのプロトタイプが吸収され、CD-NP には 7 つのプロトタイプが吸収され、CD-HP には 8 つのプロトタイプがありました。 M21 は CD-NP の糞便群でのみ検出され、M38 と M51 は CD-HP の尿群でのみ検出されました。 代謝物と比較すると、血漿、尿、糞便中の同一代謝物はそれぞれ 4、42、21 個でした。 CD グループでは 34 個の代謝物が吸収され、CD-NP では 39 個、CD-HP グループでは 40 個の代謝物が吸収されました。 M5、M7、M40、および M52 は CD-NP グループでのみ検出され、M24、M41、および M48 は CD-HP グループでのみ検出されました。
CD のさまざまな加工製品では、活性化合物の吸収および代謝に変動が観察されました。 図 14 から、HT 硫酸抱合体 (M17) の強度が尿中で最も高く、次に 3-HPP 硫酸抱合体 (M29)、メチル化 HT 硫酸抱合体 (M22)、脱ヒドロキシル化 CA 硫酸塩が続くことがわかりました。共役 (M32)、および 3,4- ジヒドロキシ ベンゼン プロピオン酸硫酸塩共役 (M19)。 処理グループの代謝産物の含有量は、特に M22、M29、M27、M16、M19、M1、および M2 で CD グループよりも高かった。 ヒドロキシチロソールなどのそれらの前駆体化合物は、抗腫瘍、抗炎症、抗菌、チウイルス、抗真菌特性を持っています [23]。 カフェイン酸は、抗炎症作用、抗がん作用、抗ウイルス作用を持っています[24]。 これは、CD およびその加工製品の臨床使用と一致していました。

議論
CD は TCM であり、PhG、イリドイド、多糖類などの主要な生理活性成分がさまざまな研究によって記録されています。 中医学の臨床現場では、CD の加工品が生のものよりも広く使用されています。 加工中に化学組成が変化し、薬効が変化する可能性があります(図14)。
PhG は、アグリコンとしてヒドロキシフェニルエチル部分を持つグルコピラノシド構造を特徴とするフェノール化合物の一種です。 これらの化合物は、多くの場合、それぞれエステル結合またはグリコシド結合を介してグルコース残基に結合したカフェイン酸およびラムノースを含みます。 今回の研究では、CD、CD-NP、CD-HPの定性分析が行われ、フェニルエタノイド配糖体(PhG)やイリドイドなどを含む計97種類の化合物が同定された。 得られた結果は、処理前後の化学組成の変化を示しました。 アクテオシド、シスタノシド C、カンネオシド II、オスマントゥシドなど、8-O- -d-グルコピラノシル部分に 4'-O-カフェオイル 基を持つ PhG の強度は処理後に減少しましたが、 8-O- -d-グルコピラノシル部分の 6'-O-カフェオイル基 (イソアセトシド、イソシスタノシド、イソカンネオシド I、イソマルチノシドなど) が、特に CD-NP グループで増加しました。 構造が 6'-O- -d-グルコピラノシル部分を有するエキナコシドおよびシスタノシド B の強度も増加しました。 2'-アセチル基を有する PhG は、チューブロシド B や 2- アセチルラクテオシドのように、プロセス中の加水分解反応により減少することがよくあります。

CD およびその加工品を経口投与した後、生体内で吸収される代謝産物の調査を実施しました。 フェーズ II の代謝プロセスが重要なカスケードであり、代謝産物のほとんどは硫酸塩、グルクロニド、およびメチル化複合体でした。 フェニルエタノール配糖体は、経口吸収および利用が低いです。 Tey は血中に吸収されにくく、生体内での代謝活性化後に前駆細胞として機能し、その役割を果たします。 ヒドロキシチロシン(HT)やカフェイン酸(CA)、その誘導体3-ヒドロキシフェニルプロピオン酸(3-HPP)などのフェニルエタノールアグリコンに生成されるフェニルエタノイド、これらの代謝物は血漿に吸収されやすく、より優れた薬効を発揮する可能性があります。効果。
ほとんどの代謝産物はラット血漿中では低濃度で検出されるか、検出されませんでしたが、尿中にはより高濃度が観察され、代謝産物が尿を介して容易に排出されることが示されました。 表 3 に示すように、同じ化合物がさまざまなグループで測定されましたが、代謝産物の濃度にはかなりのばらつきが見られ、これは CD およびその加工製品の不均一な有効性に関連している可能性があります。 尿中では HT 硫酸抱合体 (M17) の強度が最も高く、次に 3-HPP 硫酸抱合体 (M29)、メチル化 HT 硫酸抱合体 (M22)、脱ヒドロキシル化 CA 硫酸抱合体 (M32)、および 3、{{ 8}}ジヒドロキシベンゼンプロピオン酸硫酸塩共役(M19)。 処理グループの代謝産物の含有量は、特に M22、M29、M27、M16、M19、M1、および M2 で CD グループよりも高かった。
一般に、標的臓器への曝露量が多い成分は効果がある可能性があります。 十分な量のフェニルエタノイドおよびその誘導体が in vitro で評価および測定されています。 特徴的な化合物であるアクテオシドは、酒処理後に含有量が減少し、それに応じてイソアクテオシド、イソシスタノサイド C、イソカンネオシド I の含有量が増加しました。 CA や HT 誘導体などの PhG の分解生成物は生体サンプルで評価でき、米ワイン処理により in vivo での代謝産物の吸収を高めることができます。

結論
この研究では、CD およびその加工品の抽出物から 97 種類の化合物が検出されました。 いくつかの配糖体の分解は高温下で起こり、その結果、いくつかの新しい異性体と複合体が合成されました。 in vivo 研究では、ラットの血漿、糞便、尿中のプロトタイプ成分 (10) と代謝物 (44) が決定または暫定的に評価されました。 第 II 相代謝プロセスが重要なカスケードであり、ほとんどの代謝産物は HT、CA、およびその誘導体である3-ヒドロキシフェニルプロピオン酸3-HPP などのエキナコシドまたはアクテオシドと関連していました。 これらの代謝産物は血漿への吸収がより容易になり、より優れた薬効を発揮する可能性があります。 得られた結果は、CD の化学組成が異なり、in vitro と in vivo での化合物の性質に影響を与えることを示しました。




略語
PhG: フェニルエタノイド配糖体。 CD: キスタンケ・デザートティコーラ; CMM: 中国マテリアメディカ。 TCM: 伝統的な中国医学。 CD-NP: カンクサ 常圧下で酒で蒸して加工したもの。 CD-HP:Cistanche desserticola 米酒を用いて高圧下で蒸して加工。 UPLC-Q-TOF-MSE: TOF-MSE と組み合わせた超高速液体クロマトグラフィー。 PCA: 主成分分析。 VIP: 投影の重要度は変動します。 CA: カフェ酸; HA: ヒドロキシチロソール。
謝辞
適用できない。
著者の寄稿
LZ、LBN、SJ が草稿と原稿執筆に参加しました。 RJ と LPP は動物実験を支援し、すべての図と表を起草して完成させました。 ZC、HY、および JTZ は、この研究の設計と実施を支援し、原稿をレビューしました。 著者全員が最終原稿を読んで承認しました。
資金調達
この研究は、中国国家自然科学財団 (助成金番号: 81874345) および遼寧省自然科学財団 (助成金番号: 2020-MS-223) によって支援されました。
データと資料の入手可能性
現在の研究中に使用および/または分析されたデータセットは、合理的な要求に応じて責任著者から入手できます。
宣言
倫理の承認と参加への同意
この研究に実験動物を使用するための倫理的承認は、遼寧中医薬大学の医倫理委員会から得られています (承認番号: 2018YS(DW)-044-01)。 この研究におけるすべての実験手順は、遼寧中医薬大学の医療倫理委員会の倫理基準に従って行われました。
掲載の同意
適用できない。
競合する利益
著者らは、開示すべき利益相反がないことを宣言します。
著者詳細
1中国遼寧省大連の遼寧中医薬大学薬学部。 2 Monos Group の薬物研究所、ウランバートル 14250、モンゴル。
参考文献
1. 中国薬局方委員会。 中華人民共和国薬局方、vol. I. 北京: 中国医科学出版; 2020.p. 140.
2. Li Z、Lin H、Gu L、Gao J、Tzeng CM。 Herba Cistanche (Rou Cong-Rong): 伝統的な中国医学の最高の医薬品ギフトの 1 つ。 フロントファーマコル。 2016;7:41。
3. Liu BN、Shi J、Zhang C、Li Z、Hua Y、Liu PP、Jia TZ。 新鮮なカンクのさまざまな乾燥処理方法がその成分含有量に及ぼす影響。 J・チン・メッド・メーター。 2020;10:2414–8。
4. Liu BN、Shi J、Jia TZ、Lv TT、Li Z. Citanches Herba の高圧蒸しプロセスの最適化。 Chin Trad Patent Med. 2019;11:2576–80。
5. Fan YN、Huang YQ、Jia TZ、Wang J、La-Sika、Shi J。D-ガラクトース誘発性老化ラットの抗老化機能と免疫機能に対する処理前後のカンクサの効果。 チン・アーチ・トラッド・チン・メッド、2017年。 11:2882–2885。
6. Gao YJ、Jiang Y、Dai F、Han ZL、Liu HY、Bao Z、Zhang TM、Tu PF。 カンクサ YCMa の下剤成分に関する研究。 現代のチン医学。 2015;17(4):307–10。
7. Liu BN、Shi J、Li Z、Zhang C、Liu P、Yao W、Jia T。グルココルチコイド誘発ラットモデルにおけるカンクサとその米酒蒸し製品の神経内分泌免疫機能に関する研究。 Evidベースの補体代替医学。 2020;22:5321976。
8. Guo Y、Wang L、Li Q、Zhao C、He P、Ma X。中高温で急速に乾燥させたカンサスハーブによるマウスモデルにおける腎臓の活性化機能の強化。 Jメッドフード。 2019;22(12):1246–53。
9. Wang T、Zhang X、Xie W. Cistanche desserticola YC Ma、「砂漠高麗人参」のレビュー。 J・チン・メッドです。 2012;40(6):1123–41。
10. Fu Z、Fan X、Wang X、Gao X. Cistanches Herba: その化学、薬理学、および薬物動態特性の概要。 J エスノファーマコル。 2018;219:233–47。
11. Lei H、Wang X、Zhang Y、Cheng T、Mi R、Xu X、Zu X、Zhang W. Herba Cistanche (Rou Cong Rong): 植物化学と薬理学の総説。 ケムファームブル。 2020;68(8):694–712。
12. Geng X、Tian X、Tu P、Pu X。パーキンソン病のマウス MPTP モデルにおけるエキナコシドの神経保護効果。 Eur J Pharmacol. 2007;564:66–74。
13.Deng M、Zhao JY、Ju XD、Tu PF、Jiang Y、Li ZB。 神経細胞におけるTNFα誘導性アポトーシスに対するチューブロシドBの保護効果。 アクタファーマコルシン。 2004;25(10):1276–84。
14. Nan ZD、Zhao MB、Zeng KW、Tian SH、Wang WN、Jiang Y、Tu PF。 タリム砂漠で栽培されたニクイリドの茎から得られる抗炎症性イリドイド。 チン・J・ナット・メッド 2016;14(1):61–5。
15. Nan ZD、Zeng KW、Shi SP、Zhao MB、Jiang Y、Tu PF。 タリム砂漠で栽培されるカンクイの茎から得られる、抗炎症作用のあるフェニルエタノイド配糖体。 フィトテラピア。 2013;89:167–74。
16. 森川 T、パン Y、二宮 K、井村 K、袁 D、吉川 M、早川 T、村岡 O。Cistanche tubulosa 由来のイリドイドおよび非環式モノテルペン グリコシド、カンカノシド L、M、N、O、および P。 ケムファームブル。 2010;58(10):1403–7。
17. Li SL、Song JZ、Qiao CF、他。 多変量統計解析を備えた UHPLC-TOF-MS により、生の黄根と加工された黄根を区別するための潜在的な化学マーカーを迅速に探索するための新しい戦略。 J ファーム バイオメッド アナル。 2010;51(4):812–23。
18. Peng F、Chen J、Wang X、Xu CQ、Liu TN、Xu R. 蒸気処理によるニクのスライスにおけるフェニルエタノイド配糖体のレベル、抗酸化活性、およびその他の品質特性の変化。 ケムファームブル。 2016;64:1024–30。
19. マ・ZG、タン・YX。 Desertliving Cistanche でのワインの蒸し時間による 6 つのフェニルエタノイド配糖体の含有量の変化。 Chin Trad Patent Med. 2011;33(11):1951–4。
20. Peng F、Xu R、Wang X、Xu C、Liu T、Chen J. 天日乾燥中の薬用収穫後のカンクサの品質に及ぼす蒸しプロセスの影響。 バイオルファームブル。 2016;39(12):2066–70。
21. Cui Q、Pan Y、Zhang W、Zhang Y、Ren S、Wang D、Wang Z、Liu X、Xiao W. 食事性アクテオシドの代謝物: プロファイル、単離、同定、肝保護能。 J 農業食品化学。 2018;66(11):2660–8。
22. Cui Q、Pan Y、Bai X、Zhang W、Chen L、Liu X. UPLC-ESI-Q-TOF に基づく、ラットの血漿、胆汁、尿および糞便中のカンカ菌由来のエキナコシドおよびアクテオシドの代謝物の系統的特性評価-MS。 バイオメッドクロマトガー。 2016;30(9):1406–15。
23. Bertelli M、Kiani AK、Paolacci S、Manara E、Kurti D、Dhuli K、Bushati V、Miertus J、Pangallo D、Baglivo M、Beccari T、Michelini S. ヒドロキシチロソール: 有望な薬理活性を持つ天然化合物。 Jバイオテクノロジー。 2020;309:29–33。
24. Touaibia M、Jean-François J、Doiron J. カフェ酸、多用途ファーマコフォア:概要。 Mini Rev Med Chem. 2011;11(8):695–713。
詳細については: david.deng@wecistanche.com WhatApp:86 13632399501














![]()



