パート2:系統的レビューとメタアナリシスを使用した慢性腎臓病患者の痛みの有病率
Mar 10, 2022
クリックここパート1の
コンタクト:joanna.jia@wecistanche.com/ WhatsApp:008618081934791

神経因性疼痛
合計3384人の個人を含む12の研究がグループ化され、神経障害性の世界的な有病率が得られました。痛み0パーセント(95パーセントCI:6パーセント–15パーセント)(図6)で、次のように定義されたサブグループ間に有意差はありません。慢性腎臓病管理戦略(P¼{{0}}。51)。 非常に一貫した推定値(I2¼0パーセント)を持つ2つの研究を含むKTRサブグループを除いて、不均一性は世界的に高かった(I2¼95パーセント)。

![]()
メタ回帰は、サンプル中の高血圧の影響を受けた参加者の割合が高いことと、平均BMIが高いことの両方が、神経障害性の有病率の上昇と関連していることを示しました。痛み(補足図S2AおよびB;P0。002およびP<0.0001)。 予測因子として高血圧とbmiを使用した単変量モデルでは、説明されていない不均一性がそれぞれ14%と0%しか残っておらず、強い関係が示唆されています(補足表s11)。="" これらの関連付けは、年齢、性別、および地理的領域を制御する多変量モデルに残りました。="">痛み年齢、性別、および地理的領域を制御した後(補足表S11;P¼0 .03;I2¼61パーセント)。
最後に、単変量メタ回帰は、研究サンプル中の女性被験者の割合が神経障害性の有病率と負の関連があることを示しました痛み(補足表S11および補足図S2C)。
特定の身体部位に影響を与える痛み
補足表S12は、いくつかの身体部位および線維筋痛症について得られたプールされた有病率をまとめたものであり、慢性腎臓病 経営戦略。 筋骨格痛み最も一般的であるように見えた痛み非透析患者の症状慢性腎臓病 (42%; 95%CI:28%–56%)および透析(45%; 95%CI:36%– 55%)が、KTR間ではそれほど重要ではありませんでした(18%; 95%CI:6%–44%)。 線維筋痛症の有病率が非常に高いことは注目に値します。慢性腎臓病 (11%; 95%CI:8%–14%)、以前のメタ分析で報告された一般人口の推定有病率1.78%(95%CI:1.65%–1.92%)よりもはるかに高いが、より一致しているで治療された患者の間で観察された6.30パーセント(95パーセントCI:4.60パーセント–7.90パーセント)の有病率で血液透析.28 KTRの中で、最も一般的な症状は腹部であるように見えた痛み(41パーセント; 95パーセントCI:7パーセント– 86パーセント)有病率は慢性腎臓病 非透析(15パーセント; 95パーセントCI:2パーセント–63パーセント)および透析(16パーセント; 95パーセントCI:10パーセント–24パーセント)サブグループ。 の影響について透析モダリティ、腹部を調査する3つの研究痛みで治療された患者の間で血液透析または腹膜透析識別されました。 それらのうちの2つ29,30は、血液透析一方、third31は大きな違いはありませんでした。 これらの3つの研究を一緒にプールした後、ランダム効果メタアナリシスは2つのモダリティの間に違いを示しませんでした(サブグループの違いのc2テスト:P¼0。7)(図7)。
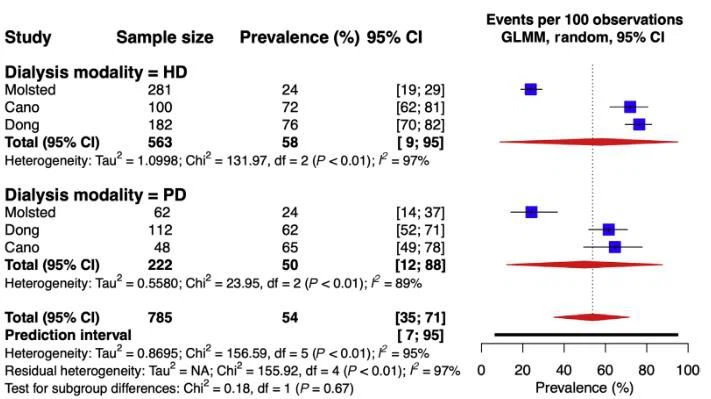
![]()
その他の部位特異的疼痛に関しては、2件の研究7,31で治療された患者の間で頭痛の同様の有病率を報告しました血液透析と腹膜透析。 線維筋痛症を調査する研究において、Berber等。32 間に有意差は見つかりませんでした透析Sarginetal。33受けている患者の間でより高い有病率を報告しました血液透析。 メタ回帰分析では、平均年齢が高いほど線維筋痛症の有病率が高いことが示されました(補足図S3、P¼0 .05;I2¼58パーセント)。

で治療された患者の間の頭痛の同様の有病率血液透析と腹膜透析が見つかり、cistancheはおそらくリリースするのに役立ちます痛み腎臓に利益をもたらします。
研究の質
補足表S13およびS14は、ニューカッスル-オタワスケールによって評価された3つのドメイン(選択バイアス、交絡、および結果測定バイアス)の各項目の研究レベルでの品質評価を示しています(補足資料S2を参照)。 研究の大部分(51%)は中程度の品質でしたが、24%と25%はそれぞれ低品質と高品質でした。 中程度の質の研究の大部分は、結果測定バイアスのリスクが全体的に低いが、選択バイアスのリスクが高いことで説明できます。 実際、ほとんどの研究(54%)は、単一のセンターから参加者をサンプリングしたため、この特定の施設に通う患者とその特定のユニットで実施された診療のみを表しています。 研究の半分では、回答率は特定できず、22の研究の中で回答率が報告されました。<80%, only="" 5="" demonstrated="" the="" representativeness="" of="" their="" responders="" either="" by="" showing="" they="" were="" no="" different="" from="" nonresponders="" or="" by="" comparing="" them="" to="" the="" larger="" population="" they="" were="" sampled="" from.="" finally,="" random="" sampling="" was="" only="" used="" in="" a="" minority="" of="" articles="" (12%).="" consecutive="" sampling="" was="" pre-dominant,="" probably="" to="" obtain="" a="" larger="" sample="" size,="" especially="" for="" studies="" recruiting="" patients="" from="" a="" single="" center.="" in="" nearly="" one-half="" of="" the="" studies="" included="" (n="" 48)="" the="" impact="" of="" confounding="" related="" to="" variables="" such="" as="" age,="" sex,="">慢性腎臓病 ステージ、または透析モダリティは考慮されませんでした。 結果測定バイアスに関しては、自己申告による品質は満足のいくものでした。痛みゴールドスタンダードと見なされている評価は、ほとんどの研究者によって選択されました(89パーセント)。 医療専門家による代理評価を使用したのは4人だけでした34,35または介護者、36,375取得痛み医療記録による診断、38–42,2つは両方の方法の組み合わせを使用しました。43,44一般的な調査の研究では痛み, 4332人が自己記入式の質問票に依存している間、彼らの評価はインタビューに基づいていた。 神経障害性を評価するために特定のツールを使用した研究は1つだけであることに注意する必要があります痛み(神経障害性の症状と徴候のリーズ評価、S-LANSS)。45他の研究は、このタイプのために特別に設計されていないスケールに依存していました痛みブリーフなど痛み在庫またはマギル痛みアンケート、医療記録からの報告、38,46または医師による決定26,47または神経内科医。41 ほとんどの場合、研究者は神経障害性の診断がどのように行われるかについて正確に言及していませんでした痛み作られた。48–53非特異的使用の場合痛みスケール、それはタイプを説明するために患者によって選ばれた質問票の言葉によって推測されたかもしれません痛み神経障害性の診断を概算するために、しびれ/うずき/灼熱の症状が時々使用されるため、経験豊富痛み.54 研究の質によって層別化されたメタアナリシスは、痛み低、中、または高品質の研究間の有病率の推定値(補足表S15;サブグループの違いに関するc2テスト:P 0 .2 for痛み; 慢性の場合はP0。09痛み; P 0 .13、神経障害性の場合痛み)。 同様に、調査したすべての結果について、有病率の推定値は、質の低い研究を除外した後も変わらず(補足表S15)、含まれる研究の全体的な質に関するいくつかの懸念にもかかわらず、これは私たちの証拠の累積レベルに影響を与えなかったようです。プールされた見積もり。

多くの患者が苦しんでいます慢性腎臓病、 とcistanche症状を改善し、保護します腎臓機能.
出版バイアスBeggのテストでは、出版バイアスの証拠は見つかりませんでしたが、Eggerのテストでは、痛みと神経障害性痛み慢性ではありません痛み。 最近層別化するとき痛みに慢性腎臓病 サブグループ、非対称性は透析グループ(補足図S4およびS5)。
この文脈で、有病率研究における出版バイアス評価の適切性の欠如を知っているので、私たちの結果が高レベルの出版バイアスによって影響を受ける可能性は非常に低いと私たちは信じています。
証拠のレベル
全体的な有病率の推定値の確実性は、痛み(不一致とバイアスのリスクのため)、慢性的に中程度痛み(バイアスのリスクがあるため)、神経障害性の場合は非常に低い痛み(不整合、バイアスのリスク、および間接性のため)。 感度分析では、ニューカッスル-オタワスケールによると、質の低いまたは中程度の研究を含めることは、プールされた推定値または不均一性レベルに影響を与えなかったことが示されましたが、選択バイアス。 確かに、参加者は、より広い範囲を代表していると見なすことができなかった集団からサンプリングされることが多すぎました慢性腎臓病 単一のセンターからの募集とランダムサンプリングのまれな使用による人口。 ダウングレードは、調査中の研究全体で観察された高い不均一性レベルからも生じました痛みと神経障害性痛み。 非特異的ツールを介した神経因性疼痛の間接的評価も、この結果のプールされた推定値の信頼度を低下させました。 サイト固有について痛み、不均一性とバイアスのリスクが有病率の推定値への信頼を再び制限したため、線維筋痛症を除くすべての結果に低レベルのエビデンスが割り当てられました。 I2が低いため(全体で74%、KTRの中で0%、透析サブグループ)、確実性は線維筋痛症の中等度と見なされました。 GRADEテーブルは、一般的な痛みの結果については補足表S16で、部位固有の痛みの結果については補足表S17で利用できます。
感度分析
地理的領域の影響を調査する感度分析の結果と痛み目盛りは、補足資料S3、補足表S18、および補足図S6〜S8で入手できます。
討論
慢性腎臓病の患者では高い痛みの負担が観察され、全体的な推定有病率は急性の痛みで60%、慢性の痛みで48%、神経障害性の痛みで10%でした。 KTRは、透析を受けている患者(63%; 95%CI:57%–68%)や慢性腎疾患の非透析患者(63%)よりも痛みが少ない(46%; 95%CI:37%–56%)ようでした。パーセント;95パーセントCI:55パーセント–70パーセント)、しかしこのサブグループでは特に高レベルの腹痛が見られました(41パーセント; 95パーセントCI:7パーセント– 86パーセント)。 透析を受けている、または保守的に管理されている患者の中で、筋骨格痛の優勢が観察され、両方のグループで同様の有病率でした(それぞれ45%と42%)。 透析治療に対する腎臓移植の利点は、研究者が全体的に低い死亡率とより良い生活の質を報告した以前の系統的レビューで強調されています。55 いくつかの研究では、慢性腎臓病の非透析と比較して、KTRグループの疼痛スコアが優れていることも報告されています56および血液透析グループ。56,57ただし、KTRのほぼ半分が依然として何らかの形の痛みを報告していることを強調しておく必要があります。これは、一般集団で観察されるよりも高いままの実質的な有病率です。 また、長期的な痛みの有病率を観察しました。慢性腎臓病の人口のほぼ半分が慢性的な痛みに苦しんでおり、10%が神経障害性の痛みに苦しんでいます。 比較のポイントとして、慢性的な痛みは世界中の一般人口の20パーセントに影響を与えると推定されています。58 国際疼痛学会によると、神経障害性疼痛は6.9%から10%の範囲であり、慢性腎臓病の人口は一般的な人口の推定値の上限に位置しています。59
我々の結果は、血液透析または腹膜透析を受けている患者の痛みの有病率が類似していることを示唆している。 腹痛や頭痛などの部位特異的な痛みの有病率も同じである可能性があります。 慢性腎臓病の病期による層別化は、慢性腎臓病の病期3および4の患者が、保守的に管理された腎不全の患者と同じくらい苦しむ可能性があることを示しました。 保守的に管理された慢性腎臓病ステージ5の患者に適応した緩和ケアの実施は、このサブグループ内の痛みの負担をわずかに減少させるようでした。 使用された多数の異なるスケールは大きなサブグループを可能にしませんでしたが、疼痛評価ツールによる層別化は、観察された研究間の不均一性の一部をうまく説明しました。 異なる表現(たとえば、Brief Pain Inventory Short Formのこれらの日常的な種類の痛み以外の痛み、EuroQol 5ディメンションの痛みまたは不快感)、およびさまざまな想起期間(たとえば、Edmonton症状評価システムの過去24時間) 、緩和ケア転帰尺度の過去3日または7日-症状腎)多種多様な疼痛ツールで使用されたものは、観察された不均一性のかなりの部分を説明する可能性があります。 ほとんどの研究者は、痛みや慢性の痛みを調査するときに検証済みの尺度を使用しましたが、神経障害性の痛みを評価するときはそうではありませんでした。 実際、含まれている12の研究のうち1つだけが、S-LANSS、神経因性疼痛質問票、またはDouleur Neuropathique 4質問など、神経因性疼痛を調査するために特別に設計されたツールとして定義された適切なツールに依存していました。
高血圧とBMIの上昇は、どちらも神経因性疼痛の有病率の上昇と有意に関連していた。 多変量解析では、糖尿病患者の割合と神経因性疼痛の有病率との間に関連性があるという証拠も見つかりました。 糖尿病性ニューロパチーは糖尿病の一般的な合併症であるため、この発見は驚くべきことではありません。 1型糖尿病患者のグループで実施された以前の研究では、高血圧も神経因性疼痛の一因となっていることがわかりました。60 神経伝導を損なうことによって。61BMIとの関連は、肥満がリスクを高めることを示唆する以前の証拠と一致しています62と強度63おそらく神経損傷を誘発する全身性炎症のメカニズムを介して、神経因性疼痛の。 以前の研究では、血液透析で治療された患者の中で最も頻繁な痛みの症状として筋骨格痛が報告されていました。64 私たちの分析では、これは慢性腎臓病の非透析と透析サブグループの両方で最も一般的な痛みのタイプです。 筋骨格には骨/関節の痛みが含まれるため、これは慢性腎臓病に関連している可能性があります-ミネラルおよび骨の障害、カルシウムとリンの恒常性の障害につながる慢性腎臓病の一般的な合併症であり、二次性副甲状腺機能亢進症を引き起こします。 結果には、骨と関節の痛み、および骨の構造と代謝の変化に関連する骨折のリスクが高くなります(KTRでは一般集団と比較して最大4倍)。65慢性腎臓病の症状-ミネラルおよび骨の障害は、慢性腎臓病の進行した段階で現れることが多く、これは、私たちが含めた研究における骨/関節の痛みの高い有病率を説明する可能性があります。66 このタイプの痛みの評価と認識は、従来の鎮痛療法とは異なる特定の治療が必要になる可能性があるため重要です。最近の証拠では、腎臓移植後の骨の痛みがビスホスホネートに反応する可能性があります。65
KTRで観察された腹痛の優勢と高い有病率は、免疫抑制療法のよく知られた副作用に関連している可能性が高く、ミコフェノール酸モフェチルで治療された患者の間で特に頻繁に起こる可能性があります67とシロリムス。68 これらの高レベルの腹痛の原因となる潜在的な根本的なメカニズムには、持続的な術後の痛みが含まれます。 内臓痛覚過敏; 粘膜損傷、潰瘍形成、憩室症、および最悪の場合の穿孔につながる免疫抑制薬の固有の毒性;69または1日あたりの投薬数の多さ。67
私たちの知る限り、これはすべての痛みの表現型と慢性腎臓病の管理戦略を含む最初の系統的レビューとメタアナリシスです。 公開済みおよび未公開のデータを徹底的に検索し、幅広い包含基準を使用することで、トピックを可能な限り広範囲にカバーし、高い統計力を実現することができました。 さらに、バイアスのリスクが高い研究を除外すると、全体的な有病率の推定値が変わらないことを示すこともできました。 使用された透過的な方法論と実施された感度分析の数は、有病率の推定値の一貫性と信頼性を保証しました。
ただし、いくつかの制限に注意する必要があります。 さまざまな研究が含まれ、慢性腎臓病患者の痛みの有病率を具体的に調査するものもあれば、さまざまな症状を報告し、痛みに厳密に焦点を当てていないものもあり、報告の精度が低く、標準化されていないことがよくあります。 さまざまな痛みの定義、想起期間、および痛みの評価尺度を伴う痛みの評価方法の標準化の欠如が、説明されていないままの実質的な不均一性の原因である可能性があります。 一部の研究では報告された特性が不足しているため、メタ回帰を常に実行できるとは限りませんでした。 それは私たちの有病率の推定に影響を与えていないように見えましたが、研究の質には一貫性がなかったことに注意する必要があります。 多くは単一のセンターで実施され、非常に少数の研究者(13%)がランダムサンプリングを使用し、応答者と非応答者の特性を比較して、一般に高いサンプリングバイアスをもたらしました。 面接は社会的望ましさのバイアスにつながる可能性がある一方で、自己記入式の質問票は高レベルの痛みを経験しているより多くの体調不良の患者によって記入されない可能性があるため、結果測定バイアスも結果に影響を与えた可能性があります。 補助なしで質問票に回答できる患者に調査を制限する透析研究は、不正確な結果につながる可能性があることが示され、インタビューを使用した評価が研究者によって推奨されました70。GRADEスコアリングによると、プールされたすべての推定値に割り当てられました。本書に記載されている理由により、非常に低いレベルから中程度の範囲の証拠のレベル。 したがって、慢性疼痛の真の有病率が私たちの推定値に近い可能性が高い場合、神経因性疼痛ではおそらく著しく異なります。 したがって、神経因性疼痛を評価するために特別に設計されたツールを使用して、代表的なサンプル間で実施されるさらなる証拠が必要です。
慢性腎臓病の患者、特に慢性腎臓病の非透析サブグループと透析治療を受けた患者では、痛みの負担が高く、生活の質に対する腎移植の利点が強化されています。 しかし、腎臓移植レシピエントの痛みの負担は重要ではありません。 包括的な痛みの評価は、検証された尺度に依存する必要があります。 この一般的な症状の認識を高めることは、その有病率を減らし、患者のグループで不必要な苦痛を防ぐために不可欠です。
生活の質は慢性腎臓病によってすでに変化しています。

の負担として痛み患者の慢性肝臓疾患非常に高い場合、重要なポイントはリリースすることです痛み、腎臓機能を改善し、患者の生活の質を改善します。Cistanche腎臓を保護し、改善することができます腎臓機能.
開示
すべての著者は、競合する利益を宣言しませんでした。
謝辞
ELは博士号を取得します。 ダンディー大学からの学生。
補足資料
補足ファイル(PDF)
表S1。 MEDLINE検索戦略。
補足資料S1。 データ抽出スプレッドシートに含まれるアイテムのリスト。
補足資料S2。 横断研究に適応したニューカッスル-オタワスケール。
補足資料S3。 感度分析の方法と結果。
表S2。 いくつかの研究と参加者は、一般的な痛み(A)と部位特異的な痛み(B)の各結果に含まれていました。
表S3。 痛みに関するメタアナリシスに含まれる研究の概要。 表S4。 慢性疼痛のメタアナリシスに含まれる研究の概要。
表S5。 神経因性疼痛のメタアナリシスに含まれる研究の概要。
表S6。 筋骨格痛のメタアナリシスに含まれる研究の概要。
表S7。 頭痛のメタアナリシスに含まれる研究の概要。
表S8。 腹痛のメタアナリシスに含まれる研究の概要。
表S9。 胸痛のメタアナリシスに含まれる研究の概要。
表S10。 線維筋痛症のメタアナリシスに含まれる研究の概要。
表S11。 疼痛、慢性疼痛、および神経因性疼痛の単変量および多変量モデルの結果を示すメタ回帰。 図S1。 Frazaoらによる範囲外の研究を削除した後の慢性腎臓病管理戦略によって層別化された慢性疼痛のフォレストプロット。
図S2:(A)高血圧、(B)平均BMI、および(C)研究サンプルの女性の割合によって影響を受けた患者の割合による神経因性疼痛の有病率のバブルプロット。
表S12。 特定の身体部位および線維筋痛症に影響を与える痛みのフォレストプロットの要約。
図S3。 研究サンプルの参加者の平均年齢による線維筋痛症の有病率のバブルプロット。
表S13。 全体的な研究レベルのバイアスのリスクを伴うバイアスのリスク評価の要約—一般的な痛みを調査する研究。
表S14。 全体的な研究レベルのバイアスのリスクを伴うバイアスのリスク評価の要約—部位特異的な痛みを調査する研究。
表S15。 研究の質(バイアスのリスク)によって層別化された疼痛、慢性疼痛、および神経障害性疼痛のメタアナリシス(フォレストプロット)の要約。 図S4。 痛み(A)、慢性の痛み(B)、および神経障害性の痛み(C)のファンネルプロットは、有病率を変換しました。
図S5。 慢性腎臓病のサブグループによって層別化された痛みの有病率を報告する研究のファンネルプロット。
表S16。 一般的な痛みの結果のエビデンスのレベルを表示するGRADEテーブル。
表S17。 部位特異的な痛みの結果のエビデンスのレベルを表示するGRADEテーブル。
表S18。 地理的位置によって層別化された痛み、慢性の痛み、および神経障害性の痛みのメタアナリシス(フォレストプロット)の要約。
図S6。 慢性腎臓病-NDの患者の痛みの有病率を報告するフォレストプロットプーリング研究。痛みの評価ツールによって層別化されています。
図S7。 疼痛評価ツールによって層別化された、透析を受けている患者の疼痛の有病率を報告するフォレストプロットプーリング研究。
図S8。 疼痛評価ツールによって層別化された慢性疼痛の有病率(慢性腎疾患管理戦略とは無関係)を報告するフォレストプロットプーリング研究。
参考文献
1. Barakzoy AS、MossAH。 末期腎疾患の痛みを治療するための世界保健機関の鎮痛ラダーの有効性。 J Am Soc Nephrol 2006; 17:3198–3203。
2. Claxton RN、Blackhall L、Weisbord SD、Holley JL 維持血液透析を受けている患者の症状の治療不足。 J痛みの症状を管理します。 2010; 39:211–218。
3. Tong A、Wong G、McTaggart S、他。 慢性腎臓病の若年成人および青年の生活の質。 J小児科。 2013; 163:1179–1185.e1175。
4. Weisbord SD、Fried LF、ArnoldRMなど。 慢性血液透析患者における身体的および感情的症状の有病率、重症度、および重要性。 J Am Soc Nephrol 2005; 16:2487–2494。
5. Pham PC、Khaing K、SieversTMなど。 慢性腎臓病患者の疼痛管理に関する2017年の最新情報。 Clin Kidney J. 2017; 10:688–697。
6. Brkovic T、Burilovic E、Puljak L.慢性間欠的血液透析を受けている成人末期腎疾患患者の痛みの有病率と重症度:系統的レビュー。 患者はアドヒアランスを好む。 2016; 10:1131–1150。
7. Almutary H、Bonner A、Douglas C.慢性腎臓病のどの患者が最も症状の負担が大きいですか? 進行した慢性腎臓病の病期と透析モダリティの比較研究。 Jレンケア。 2016; 42:73–82。
8. Lambourg E、Colvin L、Bell S、Boon G、Guthrie G.慢性腎臓病患者における痛みの有病率、鎮痛薬の使用、およびそれらの有害事象:系統的レビューのプロトコル。 PROSPEROのWebサイト。 2019.次のURLで入手可能:https://www.crd.york.ac.uk/prospero/display _ record.php? RecordID156491。2021年5月12日にアクセス。
9. Ouzzani M、Hammad H、Fedorowicz Z、ElmagarmidA.Rayyan-系統的レビューのためのウェブおよびモバイルアプリ。 Syst Rev.2016; 5:210。
10. Levey AS、Eckardt KU、Tsukamoto Y、etal。 慢性腎臓病の定義と分類:腎臓病:グローバル転帰の改善(KDIGO)からの見解。 KidneyInt。 2005; 67(6):2089–2100。
、など。
