パート2:腎臓に対する硫化水素の保護効果(レビュー)
May 19, 2022
詳細についてはお問い合わせくださいtina.xiang@wecistanche.com
5.腎疾患におけるH2Sの役割
腎障害。 私たちの以前の研究では、H2Sを生成する2つの酵素であるCBSとCSEの発現レベルが、尿路閉塞後の腎組織で減少したことが明らかになりました(42)。 インビボ研究はまた、十分なH2Sを提供するためのH2Sドナーの補給が腎障害を改善することを示した(42)。 関与するメカニズムと分子経路は、研究された疾患モデルに関連しています。 腎臓の損傷は2つのカテゴリーに分けることができます:急性腎障害(AKI)とCKD.AKIは、虚血再灌流(出血性または敗血症性ショック)の結果として、または有毒物質(ヨウ素化造影剤、アミノグリコシド、シスプラチンなど)への曝露後に発生する可能性があります。CKDは、糖尿病性腎症などの糸球体および尿細管間質性病変で発生します( DN)および他の原因の中でもとりわけ高血圧性腎症(43)。
カンカニクジュヨウエキスの利点を知るには、ここをクリックしてください
虚血再灌流傷害(IRI)腎移植の過程で、腎血流の一時的な停止は急性虚血性傷害につながり、再灌流はさらに人間の腎臓への機能的および構造的損傷を強化します。腎虚血-再灌流傷害(IRI)。 動物実験では、腎虚血再灌流後、血清および組織は、他の炎症指標、有意に上昇したマロンジアルデヒド(MDA)濃度、有意に低下したスーパーオキシドジスムターゼ(SOD)とともに、著しく増加したレベルのILおよび腫瘍壊死因子-(TNF-)を示すことが示されています。活動および腎尿細管壊死; 逆に、H2SドナーであるNa、Sは、図4(44)に示すように、炎症、酸化ストレス、および腎臓の損傷を大幅に軽減することが示されています。 MDAのレベルの上昇とSODの活性の低下は、脂質過酸化を促進し、核因子-KB(NF-KB)、IL -2、およびToll様受容体-4(TLR {{11 }})、これは炎症反応を刺激し、それによって腎細胞のアポトーシスを増加させる可能性があります(45)。 CSE阻害剤であるプロパルギルグリシンまたはCBS阻害剤であるヒドロキシルアミンは、AKIとアポトーシスを悪化させ、炎症誘発性因子のレベルが高くなり、NF-xB(P65)とリン酸化(p)のレベルが大幅に上昇することが示されています。 -アポトーシスシグナル調節キナーゼ1およびp-TNFR関連因子2。これらの変化は、TLR-2およびTLR-4の発現レベルの増加を伴い、TLRを介した炎症反応およびアポトーシスを示しています。腎IRIにも関与しています(46)。
ミトコンドリアを標的としたH2SドナーであるAP39は、ドナーの腎臓移植の生存と機能を大幅に改善し、細胞のアポトーシスと壊死を減少させることが報告されています(47,48)。 H2Sは、ドナーの腎臓の凍結保存中にアポトーシスと壊死を軽減することが示されており、ミトコンドリア膜電位を調節し、活性酸素種(ROS)の産生を減らすことにより、移植された腎臓の生存率と機能を高める可能性があります(47)。 グルコースオキシダーゼによって誘発される酸化ストレスはミトコンドリア機能障害を引き起こす可能性があり、これは腎上皮細胞のATPレベルを低下させ、比較的高濃度の細胞ROSの形成を増加させ、細胞壊死を促進します。 invitroおよびinvivo実験の両方を使用した以前の研究では、AP39前処理が腎IRIに対して濃度依存性の保護効果を持ち、300 nmlの濃度で最も有意な効果が観察されることがわかりました-(48)。 AP39のH2S保護は、非特異的な外因性H2SドナーであるGYY4137よりも1、000 X高かった(47)。さらに、H2Sは、Nod2シグナル伝達経路の活性化を阻害し、タイプを抑制することにより、炎症反応を軽減する可能性があります。マクロファージスカベンジャー受容体シグナル伝達経路は、IRIから腎臓を保護するために小胞体ストレス誘発性オートファジーをアップレギュレーションします(49)。 ただし、H2Sがこれらのターゲットにどのように作用するかは不明です。

腎移植保存に関する研究はまた、AP39を補充したUW溶液中の21度での心臓死(DCD)腎臓後の寄付の長期静的保存が、長期静的と比較して腎尿細管上皮細胞の活性を増加させ、組織壊死を減少させる可能性があることを示しましたUW溶液中の4℃での保存。 しかし、実験結果はまた、AP39を補充したUW溶液が21度でのそれと比較して4度で改善された細胞保護効果を示したことを明らかにしました(50)。 これは、当クリニックで一般的に使用されている静的極低温ストレージ(SCS)および連続極低温マシン灌流と一致しています。 ただし、低温による移植臓器への損傷をよりよく防ぐために、常温の機械灌流などの生理学的温度(37°C)での臓器保存は研究に値する可能性があることに注意してください(51)。 腎機能は、低温状態で保存された腎臓と比較して、通常の生理的温度で保存された移植腎臓で改善されることが明らかになりました(52)。以前の研究では、拡張基準ドナー(ECD)からの腎臓は通常63±16の間invitroで灌流されました血漿を含まない赤血球ベースの溶液を平均温度34.6度で使用し、対照群のCSCを使用した47のECD腎臓と比較した分。 結果は、すべてのドナーの腎臓が良好な腎機能で正常に移植されたことを示しました(53)。さらに、20度でのDCDブタ移植片の正常温度以下の機械灌流は、低体温機械灌流およびSCSと比較して移植片の予後を改善することが示されました(54) 。 したがって、H2Sの影響と移植された腎臓の保存温度をさらに調査して、理想的な保存条件を決定する必要があります。
薬物腎毒性。 シスプラチンは、クリニックで広く使用されている一般的な化学療法薬です。 シスプラチンは、CSEの発現レベルをダウンレギュレーションすることにより、H _ Sの生成を妨害し、近位尿細管細胞の死を引き起こし、それによって腎毒性を引き起こすことが知られています。 HSドナーであるNaHSとGYY4137は、シスプラチンによる細胞死と腎毒性を軽減することが報告されています(55)。 以前の研究では、H2SがNAD依存性デアセチラーゼサーチュイン-3(SIRT3)のCys256、Cys259、Cys280、およびCys283残基のS-スルフヒドリル化を増加させ、その標的タンパク質であるダイナミン様120の脱アセチル化を誘導することが明らかになりました。 kDaタンパク質(OPAl)、ATPシンターゼおよびSOD2により、ミトコンドリア分裂が減少し、ATP産生が増加し、それによって酸化的損傷が減少します(56)。さらに、H2Sは、NADPHオキシダーゼの活性を阻害することにより、細胞内ROSおよびMAPKの生成を阻害する可能性があります。これは、NADPHオキシダーゼサブユニットP47PHOx(55)に対するHSの加硫効果に関連しています。 NADPHオキシダーゼ活性を低下させる一方で、H2Sは、細胞内でのROSの生成を阻害するために、核因子赤血球2-関連因子2(Nrf2)の核転座を誘発する可能性もあります。 さらなる実験により、外因性H2SドナーがAktのリン酸化とケルチ様ECH関連タンパク質1(Keapl)の二量体化を引き起こすことが明らかになりました。 Akt活性化の阻害は、Nrf2の核移行を弱めるだけでなく、外因性H2Sドナーの保護効果を低下させることが報告されています(57)。酸化防止剤遺伝子(58)。 したがって、H2Sは、Akt / KeaplおよびMAPKの活性化を介して細胞内のROS産生を阻害し、それによってNrf2の核移行を媒介すると仮定されています。 また、NADPHオキシダーゼの活性を低下させることにより、細胞内でのROSの生成を阻害する可能性があります。 最近の研究では、外因性H2Sがシクロホスファミド誘発腎毒性において腎保護の役割を果たし、Nrf2およびヘムオキシゲナーゼ-1(HO -1)などの下流の抗酸化タンパク質の発現が増加し、減少することが示されています。図4に示すように、腎組織におけるグルタチオンとSOD(57,59)。
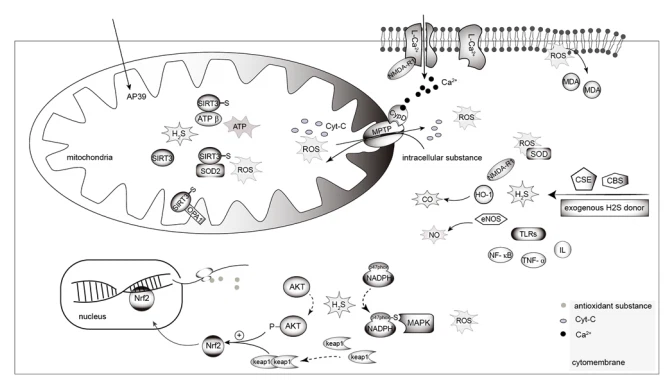
以前の研究の組織病理学的結果は、シスプラチングループの腎組織がデスミンタンパク質発現に陽性であり、顕著な有足細胞損傷、メサンギウムマトリックスの量の増加、およびメサンギウム細胞の増殖の増加を示した。 特に、NaHS療法は有足細胞の損傷を改善し、ネフリンタンパク質レベルを増加させる可能性があります(60)。 これらの発見は、H2Sが腎有足細胞を保護することによってシスプラチン誘発性腎障害を改善する可能性があることを示唆しました。 ラットのゲンタマイシン誘発腎障害では、NaHSは腎NOおよびTNF-レベルを有意に低下させ、同時に総抗酸化能(T-AOC)、HO -1、およびIL -10レベルを上昇させ、その上昇を低下させました。 eNOSレベルをアップレギュレートしながら、腎誘導性NOS(iNOS)で。 亜鉛プロトポルフィリン(選択的HO -1阻害剤)はこれらの変化を逆転させ、抗炎症薬H2S(61)の抗酸化作用。 したがって、H2Sは、部分的にCO / NO経路に依存することにより、AKIを保護する上で抗炎症および抗酸化の役割を果たしている可能性があり、このメカニズムは、主にNOレベルをダウンレギュレーションするか、COレベルを増加させることによってNOの影響をダウンレギュレーションするように機能する可能性があります(61 )。

DN。 ストレプトマイシン誘発DNラットは、明らかな腎機能低下と機能不全、SIRT1とSODの活性の低下、カスパーゼ-3、p53、MDAの相対的発現の増加を伴う、顕著な炎症と酸化ストレスを示すことが示されています。 ただし、NaHSは腎機能を改善する可能性があり、血清尿素およびクレアチニンレベルの大幅な低下、腎障害のマーカー、および前述のDNの指標の逆転として現れます(62,63)。 ATP感受性カリウム(Karp)チャネルおよびL型カルシウムチャネルは、DN腎細胞におけるROSレベルおよび酸化ストレスの増加に関連していることが示されています。 NaHSはDNのラットモデルでT-AOCを増加させ、総NOレベルを低下させる可能性があり、Kap阻害剤の使用はT-AOCをさらに増加させ、NOレベルを低下させる可能性があります(62)。 したがって、DNに対するH2Sの腎保護メカニズムは、腎組織の抗酸化物質およびNOに対するKATpチャネル活性化を介した効果に部分的に依存している可能性があります。
以前の研究では、腎損傷は高グルコース環境下のC57BL / 6JおよびAkita(C57BL / 6JIns2Akita)マウスでシミュレートされ、実験は細胞質Ca²と流入の増加、ミトコンドリアマトリックスタンパク質シクロフィリンD(CypD)の活性化を示しました、ミトコンドリア透過性遷移開口部の増加、ミトコンドリア膜電位の喪失、および酸化的バースト。 H2SドナーGYY4137は、治療後の前述の影響を軽減する可能性があります。 N-メチル-D-アスパラギン酸受容体-R1(NMDA-RI)ブロッカーMK -801でも同様の結果が観察され、H2S機能がNMDA-R1(64)に関与している可能性があることがさらに確認されました。 NMDA-R1-を介したCa2*イオンの流入を阻害することにより、細胞内Ca2を減少させ、Ca2プラス依存性CypD活性化を減少させて、ミトコンドリア透過性遷移孔の開口とミトコンドリア膜電位の喪失をもたらします。 これらの効果は、図4に示すように、ミトコンドリアの形態と機能への損傷を回避し、活性酸素物質の発生を引き起こし、糖尿病性腎臓細胞を酸化ストレス損傷から保護する可能性があります。DNに対するH2Sの保護効果を評価する用量反応実験で腎臓では、100 mol / kg /日の用量で、SIRT1の活性/発現が正常に戻り、DNラットの腎臓機能が改善されることがわかりました(63)。 ただし、この以前の研究では、SIRT1と酸化ストレスおよび炎症との関係については詳しく説明されておらず、それらの間の作用の分子メカニズムについては、さらに調査する必要があります。
腎線維化。 さまざまな要因による腎臓への長期的な損傷は、腎線維化の発生につながる可能性があります。 糖尿病ラットの腎臓では、NaHS療法により、トランスフォーミング成長因子- 1(TGF - 1)、細胞外シグナル調節キナーゼ1/2(ERK1 / 2)、メタロプロテイナーゼ(TIMP)の組織阻害剤の発現がダウンレギュレートされました。 )、およびマトリックスメタロプロテイナーゼ(MMP)、腎線維化の改善につながる(65,66)。 腎線維化は、図5に示すように、TGF- / Smadシグナル伝達、AMP活性化プロテインキナーゼ(AMPK)活性化、ERK1 / 2発現、およびMMP / TIMP調節不全(65,66)に関連しています。
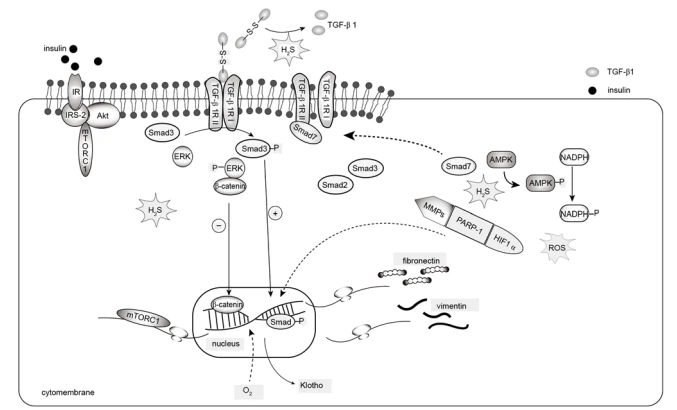
新規のH2S放出化合物であるS-プロピルシステインは、高血糖フィブリンおよびIV型コラーゲンのmRNA発現レベル、ならびにメサンギウム細胞の過剰増殖および肥大を阻害することが明らかになりました。 さらなる実験により、これがTGF- 1-およびSmad3-関連のシグナル伝達経路の阻害に関連していることが確認されました(67)。
オスのルイスラットにおける片側尿管閉塞(UUO)に続いて、H2S治療は血清クレアチニンおよび尿タンパク質/クレアチニン排泄率を低下させることが示され、組織はフィブロネクチン、ビメンチン、Smad2、TGFなどのEMT関連タンパク質の発現低下を示しました{{3 }}およびTGF- 1受容体(TR)I。 病理学的分析はまた、H2Sが皮質喪失、炎症性損傷、および腎尿細管間質性線維症を軽減することを示した(68)。 以前の研究では、H2Sを介したSmad7の発現がT RIIの発現を低下させ、内皮細胞におけるカドヘリン発現のアップレギュレーションとビメンチン発現のダウンレギュレーションを介してラットモデルのUUO腎線維化を改善する可能性があることが示されています(69-71)。 、T RIIはTRIに結合して活性化し、これにより下流のSmad発現の活性化が増加し、内皮細胞におけるビメンチン発現のアップレギュレーションとカドヘリン発現のダウンレギュレーションにつながります。 Smad7はTRI/ T RIIと相互作用して、このプロセスを防ぐことができます(70,71)。EMTを誘導するためにヒト組換え活性TGF - 1を使用したinvitro実験でも、H2SがTGFの活性二量体のジスルフィド結合を切断することがわかりました{ {16}}、および不活性なTGF - 1モノマーの形成を促進しました(72)。さらに、NaHSはTGF - 1によって誘発される-カテニンの発現の増加を減少させ、ERKのリン酸化を増加させ、 TGF- 1によって誘発される-カテニンの核移行を阻害した。 ERK阻害剤U0126または-カテニン低分子干渉RNA(siRNA)剤XAV939を使用すると、フィブロネクチン、E-カドヘリン、およびTGF-RIに対するNaHSの影響が無効になります。 これらの発見は、H2SがERK活性化と-カテニン転座を阻害することによってTGF - -誘発性EMTをブロックし、腎線維化を予防する可能性があることを示しています(73)。
糖尿病の秋田マウスでは、血漿H2S、ROSおよびそのレギュレーターROSモジュレーター1のレベル、およびコラーゲン架橋タンパク質(プロリル4-ヒドロキシラーゼサブユニットa 1およびプロコラーゲン-リジン、2-オキソグルタル酸)の発現5-ジオキシゲナーゼ2)が増加し、ポリADPリボースポリメラーゼ-1(PARP -1)、低酸素誘導因子-1(HIF -1)、およびMMP -9、-13および-14が増加しました。 これらの発見は、microRNA(miR)-194のダウンレギュレーションに関連している可能性があります。 特に、GYY4137はmiR-194の発現を回復することが示されました。 さらに、invivoおよびinvitro実験により、miR -194ミミックでトランスフェクトされた細胞が高グルコース誘発性ROS産生の軽減を示すことが明らかになりました(74)。 高グルコース環境はROSレベルを上昇させ、PARP活性化を引き起こす可能性がありますが、PARP -1欠損症はDN(75)を軽減する可能性があります。 さらに、HIF -1をブロックすると、糖尿病の腎臓における糸球体肥大、ECM沈着、および尿中アルブミン排泄が減少する可能性があります(76)。 これらの結果は、H2Sが糖尿病性腎ECM沈着を軽減し、それによってMMP / PARP -1 / HIF -1発現を調節してROSレベルを低下させ、コラーゲン架橋を増加させることにより腎線維化を軽減する可能性があることを示唆しました。
腎線維化に関与するマトリックスタンパク質含有量の増加は、AMPK活性およびインスリン受容体(IR)/ IR基質(IRS)-2 / Akt /哺乳類のラパマイシン複合体1(mTORC1)の活性化に関連していると報告されています。 )/ mRNA転写シグナル伝達軸(77)。近位腎尿細管上皮細胞では、高グルコースレベルがAMPKのリン酸化と活性を阻害し、NADPHオキシダーゼ4(NOX4)の発現と活性を増加させ、ROSの産生とマトリックスタンパク質合成を逆転させた。さらなる実験では、AMPK阻害剤はNaHSが高グルコースによって誘発されるNOX4の発現を低下させるのを防ぎました(78)。さらに、N(o)-ニトロ-L-アルギニンメチルエステル(NOS阻害剤)が明らかになりました高グルコースによって誘発されるNOX4発現のNaHS阻害を廃止することができます。 NaHSは、eNOSの代わりにiNOSの発現を強化しました。 さらなる実験により、iNOS siRNAおよび1400W(選択的iNOS阻害剤)が、高グルコース誘発性NOX4、ROS、およびマトリックスラミニン発現に対するNaHSの好ましい効果を排除することが示されました(78)。 したがって、NaHSは、NO産生を誘導し、AMPK経路を仲介して高血糖性腎線維症を抑制し、糖尿病性腎機能を保護することにより、酸化ストレスと腎間質マトリックスタンパク質の発現を調節する可能性があります。 2つのガス送信機、H2SとNO、およびそれらの相互作用は、DNの治療標的として使用できます(78)。
低酸素症と炎症は腎線維化を引き起こす可能性があり、腎低酸素症はクロトープロモーターのメチル化とサイレンシングに関連しています。 特に、NaHS治療は、低酸素症を大幅に軽減し、クロトープロモーターのメチル化を逆転させてクロトー発現を増加させ、それによってマウスの尿細管性間質性線維症を改善することが報告されています(79)。 M1 / M2マクロファージ浸潤とNLRP3インフラマソーム活性化の阻害、およびその後のNF-kBとIL -4 / STAT6シグナル伝達経路の不活性化も、腎線維化と腎に対する保護において抗炎症および抗線維化の役割を果たします。閉塞後の損傷(80)。 腎尿細管上皮細胞では、H2SはSIRT1の2つの保存されたドメイン(Cys371/374およびCys395/398)を硫化し、その標的タンパク質NF-kB(p65)およびSTAT3の脱リン酸化および脱アセチル化を誘導し、それによって酸化を減少させることが示されています高グルコースによって引き起こされるストレス、炎症、EMT(81)。 腎線維化はまた、老化と肥満に関連しています。 特に、NaHSはAMPK活性を回復し、IR / IRS -2 / Akt / mTORCl / mRNA翻訳軸の活性化を阻害し、老齢マウスの腎機能を改善しました(77)。さらに、miR-21は高齢者の腎障害に関連していることが示されています。 miR -21発現の阻害後、マウス内皮細胞におけるH2S生成酵素、CBSおよびCSEの発現レベルがアップレギュレーションされ、MMP -9およびIV型コラーゲンの発現レベルがダウンレギュレーションされました(82 )高脂肪食(HFD)誘発腎損傷モデルでは、H2Sは雄マウスの腎皮質におけるIRおよびAktのリン酸化レベルを低下させました。これは、肥満関連の腎損傷がIR/に関連していることを示唆している可能性があります。 Akt経路; しかし、この関連性は雌マウスでは観察されておらず、性関連の要因に関連しているかどうかはまだ研究されていません(83)。 さらに、H2SはHFD誘発性肥満マウスの腎臓における脂質蓄積を有意に減少させ、研究はH2SがNF-kB(P65)発現をダウンレギュレートして腎炎症を減少させ、肥満マウスのHFD誘発性腎損傷を軽減する可能性があることを示しました(84)。 これらの発見は、肥満が炎症性炎症性腎線維症および腎障害を悪化させる可能性があることを示唆した。

6.結論
H2S欠乏症は、腎疾患の発症と進行の潜在的な危険因子です。 IRI、薬物腎毒性、およびDNを含むさまざまな腎損傷は、病理学的発達中にH2Sの代謝の不均衡を示します。 外因性H2Sを補充すると、これらの疾患によって引き起こされる腎障害を軽減し、腎線維化の進行を遅らせ、腎機能を改善することができます。 H2Sが腎保護において抗酸化、抗炎症、抗アポトーシス、および抗線維化の役割を果たしているシグナル伝達経路と分子は、ますますよく理解されています。 さらに、オルガネラはAKIとCKDの進行に顕著な役割を果たします。 現在、ミトコンドリアの恒常性、ミトコンドリアのオートファジー、小胞体の酸化ストレスなどの細胞小器官への損傷に関する研究は、AKIとCKDの病理学的メカニズムに関して比較的限られており、より詳細な研究が必要です。 外因性HSドナーの観点から、ミトコンドリアを標的とし、薬剤の制御放出を誘導する薬物の研究は、AKIおよびCKDの治療に不可欠な手段を形成する可能性があります。
