糖尿病性腎疾患における尿細管間質性損傷の有用な知識--パートII
Mar 18, 2022
詳細情報:ali.ma@wecistanche.com
糖尿病性腎疾患における尿細管間質性損傷に関連する免疫関連ハブ遺伝子としての血管細胞接着タンパク質1の同定と検証
Yan Jia、et al
概要
糖尿病性腎疾患(DKD)は慢性腎臓病(CKD)および末期腎疾患(ESRD)ですが、病因は完全には理解されていません。 尿細管間質性損傷は、DKDの発症と進行に重要な役割を果たします(糖尿病性腎症)。 本研究は、尿細管間質性免疫細胞浸潤のプロファイルを調査し、DKDにおける尿細管細胞損傷と間質性炎症の間の根本的なメカニズムを明らかにすることを目的とした(糖尿病性腎症)バイオインフォマティクス戦略を使用します。 まず、xCell分析が特定されました免疫細胞DKDの重要な変更を表示する(糖尿病性腎症)ダウンレギュレーションされたCD4プラスT細胞、Th2細胞、CD8プラスT細胞、M1マクロファージ、活性化樹状細胞(DC)、従来のDC、およびダウンレギュレーションされた制御性T細胞を含む尿細管間質。 第二に、ピロトーシスは、プログラム細胞死の他の形態と比較して、細胞死の主な形態として特定されました。 血管細胞接着タンパク質1(VCAM1)は、トップランクのハブ遺伝子として同定されました。 相関分析は、VCAM1がピロトーシスと有意に正の相関があり、浸潤していることを示しました免疫細胞尿細管間質で。 DKD尿細管間質におけるVCAM1のアップレギュレーションは、European Renal cDNA Bankコホートでさらに検証され、糸球体濾過率(GFR)と負の相関関係があることが観察されました。 私たちのinvitro研究は、糖尿病条件下でのHK -2細胞におけるVCAM1発現の増加を検証し、ジスルフィラムによるピロトーシス阻害は、VCAM1発現、炎症性サイトカイン放出、および線維症を減少させました。 結論として、私たちの研究は、浸潤したと相互作用する可能性がある腎尿細管細胞におけるアップレギュレーションされたVCAM1発現を特定しました免疫細胞、したがって線維症を促進します。 FDA承認の薬剤ジスルフィラムはDKDの線維症を改善する可能性があります(糖尿病性腎症)尿細管ピロトーシスとVCAM1発現を標的とすることによって。
キーワード:DKD; 尿細管間質; 免疫細胞; ピロトーシス; VCAM1; ジスルフィラム
Cistancheは扱うことができます糖尿病肝臓疾患
腎臓機能のためのカンカニクジュヨウ粉末をクリックしてください
討論
DKDを治療するための現在利用可能な臨床的アプローチ(糖尿病性腎症)制限されたままであり、主に高血糖、タンパク尿、およびレニン-アンジオテンシン系の遮断の厳密な制御を伴います。 DKD関連のESRDの発生率が高いことを考えると、斬新で満足のいく戦略が緊急に必要とされています。 蓄積された証拠は、DKDの病因における免疫と炎症の最も重要な役割を示しています(糖尿病性腎症)。 現在までに、いくつかの研究で、DKD患者の糸球体免疫細胞浸潤に関連する遺伝子がスクリーニングされています[20]。 関連する尿細管間質性研究はまれです。 本研究では、バイオインフォマティクス分析を使用して、尿細管間質における免疫細胞浸潤と関連する細胞プロセスを分析しました。 ピロトーシスは、GSEAおよびGSVAを使用して、プログラム細胞死の他の形態の中で細胞死の主な形態として特定されました。 VCAM1は、免疫関連の最上位のハブ遺伝子として同定され、DKD患者の腎機能と相関していました。 インビトロ研究は、糖尿病条件下で培養されたHK -2細胞におけるVCAM1発現の増加を検証し、ジスルフィラムによるピロトーシス阻害は、VCAM1発現、炎症性サイトカイン放出、および線維症を減少させた。 私たちの研究は、腎近位尿細管ピロトーシス、VCAM1発現、およびDKD患者における間質性免疫応答の間の密接な関係を特定しました(糖尿病性腎症)。 この研究は、DKDの尿細管間質性病因への新しい洞察を提供しました(糖尿病性腎症)そして、新しい治療標的を特定するのに役立ちました。
xCellは、DKD患者の免疫細胞浸潤の包括的な評価を実施するために使用されました(糖尿病性腎症)。 結果は、自然免疫と適応免疫の両方がDKD患者の尿細管間質性損傷に関与していることを明らかにした(糖尿病性腎症)。 マクロファージとDCは単核食細胞(MNP)システムを構成し[21]、これは腎臓で特に複雑です[22]。 マクロファージ、特にM1マクロファージは、尿細管間質で有意に濃縮されていることがわかりました。 間質性マクロファージM1浸潤は、動物モデルとヒトの腎臓の両方で、間質性線維症、尿細管萎縮、腎機能、タンパク尿と相関していることが報告されています[23–25]。 M1マクロファージはサイトカインとタンパク質(一酸化窒素、血小板由来成長因子、IL -1、TNF-など)を産生し、血管内皮細胞に損傷を与え、線維芽細胞とメサンギウム細胞を増殖させ、間質性線維症を悪化させます[ 26]。 DCは、ループス腎炎[27,28]や半月体形成性糸球体腎炎[29,30]などのさまざまな進行性腎疾患における尿細管間質性炎症に関与していると報告されています。 それにもかかわらず、DKDや高血圧性腎症などの多くの一般的な腎疾患におけるDCの役割はよくわかっていないままです。 CD11と樹状細胞がNODマウスの糸球体に浸潤し、アルブミン尿と相関することを示した動物実験は1つだけであり[31]、間質への樹状細胞の浸潤はこれまで報告されていません。 腎臓DCの大部分は、CD11bおよびCX 3- Cモチーフ受容体1を発現する従来のDC(cDC)です[32,33]。 DC、特に活性化DCおよび従来のDCの浸潤の増加を観察し、DKDの尿細管間質性病因におけるこれらの細胞の役割を示しています。 以前の研究では、DCは尿細管間質内で形態学的に同定され、薬物誘発性急性間質性腎炎[34]および軽鎖関連尿細管間質性腎炎[35]における間質性炎症の病因に関与している可能性があることが報告されています。 特定のメカニズムには、追加の実験的証拠が必要です。 ヘルパー(CD4 plus)T細胞、細胞傷害性(CD8 plus)細胞、およびB細胞は、適応免疫システムの重要な構成要素です。 本研究では、間質におけるCD4plusおよびCD8plus T細胞の有意な濃縮を観察し、DKDにおける適応免疫の役割を示唆しています。(糖尿病性腎疾患)。動物実験では、ストレプトゾトシン治療ラットの腎臓間質にCD4plusおよびCD8plusT細胞の浸潤も検出されました[36]。 糖尿病患者では、CD4とT細胞およびCD20細胞の数がタンパク尿と正の相関を示します[37]。 ただし、すべてのCD4とT細胞がDKDを促進するわけではありません(糖尿病性腎疾患)。私たちの研究では、TregはDKDでダウンレギュレーションされ、ピロトーシスとほぼ負の相関がありました(r {{0}} -0.4191、P=0 .0522)。 制御性T細胞はDKDで保護的な役割を果たしているようです。
Cistancheは扱うことができます糖尿病肝臓疾患
腎尿細管上皮細胞は尿細管機能と糸球体機能の両方に重要であり、損傷した腎尿細管細胞は炎症性サイトカインとケモカインの重要な供給源です[38]。 複数の研究により、尿細管細胞のピロトーシス、ネクロトーシス、アポトーシス、フェロトーシスなどの調節された細胞死(RCD)が腎疾患の病態生理学に寄与することが示されています[39–42]。 データセットのGSEAとGSVAを使用してさまざまな形態の細胞死を評価し、尿細管損傷と間質性免疫細胞浸潤の関係を調べました。 結果は、ピロトーシスがネクロトーシス、アポトーシス、フェロトーシス、およびオートファジーと比較して細胞死の主な形態であることを明らかにしました。 DKD患者における活性酸素種(ROS)の蓄積(糖尿病性腎症)高血糖によって引き起こされるのは、NLRP3(NOD様受容体ファミリー、3を含むパイリンドメイン)インフラマソームの重要な活性化因子です。 次に、NLRP3はガスデルミンD(GSDMD)を活性化し、細胞膜の破裂と細胞内容物の放出を急速に引き起こし、炎症反応を引き起こします[43]。 ピロプトーシスは、アルツハイマー病[44]、パーキンソン病[45]、アテローム性動脈硬化症[46]、関節リウマチ[47]などの多くの慢性進行性疾患に関与しています。 相関分析は、ピロプトーシスがCD4 + T細胞、CD4 + Tメモリー細胞、Th2細胞、CD8 + T細胞、CD8 + Tcm細胞、CD8 + Tem細胞、Tδ細胞、NK細胞の侵入型浸潤の増加と正の相関があることを示しました。 M1マクロファージ、活性化樹状細胞、従来の樹状細胞、および好中球。 したがって、我々の研究は、尿細管ピロトーシス関連の間質性炎症がDKDの重要な原因である可能性があることを示した(糖尿病性腎症)。 この発見は、尿細管上皮細胞ピロトーシスがNLPR3インフラマソーム、IL -1、およびTGF-のレベルの増加を伴うことを示す糖尿病およびdb/dbマウスの患者の研究で確認されました。 尿細管上皮細胞ピロトーシスを標的とする治療は、DKDの進行を妨げるために重要である可能性があります(糖尿病性腎症).
サイトハバから得られたVCAM1の最高のMCCスコアは、それがDKDの重要なハブ遺伝子であることを示唆しました(糖尿病性腎症)尿細管間質性損傷。 VCAM1は、白血球の内皮への接着に重要な役割を果たします。 動物実験によると、MRL / lpl(ループス腎炎のマウスモデル)腎臓は、内皮、皮質細管、および糸球体でVCAM1発現の増加を示します[48]。 2型糖尿病の患者は、VCAM1の血清レベルが有意に上昇しており、VCAM1レベルはアルブミン尿の程度とよく相関しています[49]。 DKDのVCAM1に関する以前の研究(糖尿病性腎症)主に糸球体内皮細胞に焦点を当てています[50]。 しかし、研究者らは、VCAM1の尿細管発現がDKD患者で上昇しているかどうか、およびDKDの間質性病因に関与しているかどうかを完全には解明していません。 本研究では、DKDのアップレギュレーションされたVCAM1mRNAレベル(糖尿病性腎症)公開GEOデータセットの尿細管間質とHK-2細胞での尿細管VCAM1発現の著しい増加により、DKDでの尿細管VCAM1発現のアップレギュレーションが確認されました。 VCAM1はリンパ球と単球の接着分子であるため、本研究におけるVCAM1発現と間質性免疫細胞浸潤との正の相関は、尿細管VCAM1発現の上昇により、タンパク質が単核細胞と相互作用し、間質性線維症を促進する可能性があることを示しました。 我々の結果と一致して、急性腎同種移植片拒絶反応のエピソードにおける尿細管VCAM1発現の増加は、T細胞および単球の浸潤と関連している[50]。 さらに、VCAM1の発現とピロトーシスの間に正の相関関係があることを発見しました。これは、ピロトーシスの尿細管細胞がVCAM1を放出する可能性があることを示しています。 インビトロ研究は、糖尿病条件下で培養されたHK -2細胞におけるVCAM1発現の増加を検証し、ジスルフィラムによるピロトーシス阻害は、VCAM1発現、炎症性サイトカイン放出、および線維症を減少させた。 私たちの研究は、DKDの魅力的なターゲットとして尿細管VCAM1を強調しました(糖尿病性腎症)治療(図10)。 しかし、尿細管VCAM1と間質における免疫細胞浸潤との相互作用の根底にある分子メカニズムは本質的に不明であり、さらなる実験的研究が緊急に必要とされています[51]。
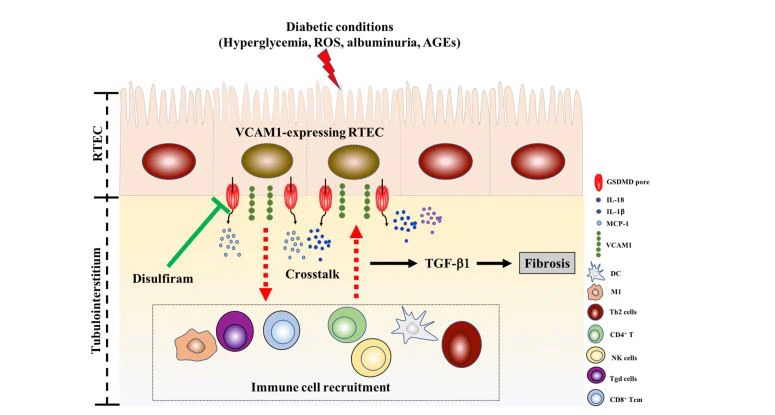
図10.DKDで間質性炎症と線維症を促進する管状上皮細胞を発現するVCAM1-の提案されたモデル(糖尿病性腎症)、およびジスルフィラムによるそれらの阻害。
現在の研究では、尿細管間質性免疫細胞浸潤のプロファイルを調査し、DKD患者のプログラム細胞死の主な形態としてピロトーシスを特定しました(糖尿病性腎症)バイオインフォマティクス分析を使用します。 分析メソッドは信頼性が高く、斬新でした。 の相関関係免疫細胞、ピロトーシス、およびVCAM1は、将来の研究のための新しい情報を提供します。 さらに、私たちのin vitro研究では、FDAが承認した薬剤のジスルフィラムが、DKD患者の尿細管ピロトーシスとVCAM1の発現を阻害することにより、間質性炎症と線維症を緩和する可能性があることが示唆されました。(糖尿病性腎症)。 ただし、この調査にはいくつかの制限があります。 まず、分析に適用されたサンプルサイズが小さかった。
第二に、詳細な実験を行っても結果が確認されなかった。 したがって、より多くの組み合わせサンプルが必要になり、結果はDKDでの実験によって検証されます(糖尿病性腎症)動物モデルとDKD(糖尿病性腎症)コホート。
結論
結論として、バイオインフォマティクス分析を使用して、尿細管間質性免疫細胞浸潤のプロファイルを調査し、DKDの尿細管間質におけるピロトーシスの役割を評価しました(糖尿病性腎症)。 VCAM1はハブ遺伝子として同定され、ピロトーシスと正の相関があり、浸潤していた免疫細胞。 さらに、VCAM1の発現は腎尿細管細胞で上昇することが検証されました。 インビトロ研究により、FDA承認薬のジスルフィラムが腎尿細管細胞のピロトーシスを抑制し、VCAM1の発現、炎症性サイトカインのレベル、および線維症を減少させることが明らかになりました。 DKD患者の尿細管間質におけるピロトーシスとVCAM1のさらなる実験的分析(糖尿病性腎症)免疫療法の標的を特定する可能性があります。
データと資料の入手可能性
研究中に使用されたデータセットは、合理的な要求に応じて対応する著者から入手できます
著者の貢献
YJはデータを分析し、結果を解釈し、記事の草稿を作成しました。 YJとZXは研究を考案、設計、組織化しました。 HXとLTがデータを分析しました。 YJとQYはinvitro実験とVCAM1免疫染色を実施しました。 ZXは結果を解釈し、原稿を改訂しました。 すべての著者が最終原稿を読み、承認しました。
資金調達
研究は、中国ポスドク科学財団(No.2018M640808)および深センの「三明」医学プロジェクト(No.SZSM201812097)からの助成金によってサポートされました。
Cistancheは扱うことができます糖尿病肝臓 疾患
参考文献
[1]ヤンC、ガオB、趙X、他。 中国腎臓病ネットワーク(CK-NET)2016年次データレポートのエグゼクティブサマリー。 KidneyInt。 2020; 98(6):1419–1423。
[2] Johansen KL、Chertow GM、Foley RN、et al .: US Renal Data System 2020 Annual Data Report:Epidemiology of Kidney Disease in theUnitedStates。 J腎臓Disです。 2021; 77(4 1):A7–A8。
[3] Zhu X、Xiong X、Yuan S、他。 糖尿病性腎症患者の新しい病理学的分類における間質性線維症と尿細管萎縮の検証:中国での単一施設研究。 J糖尿病の合併症。 2016; 30(3):537–541。
[4] Y、Xu F、Le W、etal。 糖尿病性腎症患者の腎組織学的変化と転帰。 ネフロールダイヤル移植。 2015; 30(2):257–266。
[5]ギルバートRE。 近位尿細管症:原動機と主要な治療標的糖尿病肝臓疾患。 糖尿病。 2017; 66(4):791–800。
[6] Hickey FB、MartinF.における免疫システムの役割糖尿病肝臓 疾患。 Curr Diab Rep.2018; 18(4):20。
[7] Tang SCW、YiuWH。 自然免疫糖尿病肝臓疾患。 ナットレブネフロール。 2020; 16(4):206–222。
[8] Aran D、Hu Z、ButteAJ。 xCell:組織の細胞の不均一性の状況をデジタルで表現します。 ゲノムバイオロジー。 2017; 18(1):220。
[9] Irizarry RA、Hobbs B、Collin F、他。 高密度オリゴヌクレオチドアレイプローブレベルデータの調査、正規化、および要約。 生物統計学。 2003; 4(2):249–264。
[10]LimmaSGK。 マイクロアレイデータの線形モデル。 In:Gentleman R、VJ C、Huber W、et al、編集者。 RとBioconductorを使用したバイオインフォマティクスと計算生物学のソリューション。 巻 397〜420。 ニューヨークニューヨーク:Springer; 2005.p。 2005年。
[11] Hanzelmann S、Castelo R、Guinney J. GSVA:マイクロアレイおよびRNA-seqデータの遺伝子セット変異分析。 BMCバイオインフォマティクス。 2013; 14(1):7。
[12] Subramanian A、Tamayo P、Mootha VK、他。 遺伝子セット濃縮分析:ゲノムワイドな発現プロファイルを解釈するための知識ベースのアプローチ。 Proc Natl Acad Sci US A. 2005; 102(43):15545–15550。
[13] Ritchie ME、Phipson B、Wu D、他。 limmaは、RNAシーケンシングおよびマイクロアレイ研究のための差次的発現分析に力を与えます。 NucleicAcidsRes。 2015; 43(7):e47。
[14] Chin CH、Chen SH、Wu HH、他。 cytoHubba:複雑なインタラクトームからハブオブジェクトとサブネットワークを特定します。 BMCSystBiol。 2014; 8(4):S11。
[15] Zhou Y、Zhou B、Pache L、他。 Metascapeは、システムレベルのデータセットを分析するための生物学者向けのリソースを提供します。 ナットコミュン。 2019; 10(1):1523。
[16] Zhan M、Usman IM、Sun L、他。 ミオイノシトールオキシゲナーゼによる腎尿細管ミトコンドリアの品質管理の崩壊糖尿病肝臓疾患。 J Am Soc Nephrol 2015; 26(6):1304–1321。
[17]佐藤R、宮田K、葛田A、etal。 腫瘍壊死因子-{alpha}は、ヒト腎近位尿細管細胞でp50/p50ホモ二量体を形成することによりアンジオテンシノーゲンの発現を抑制します。 J PhysiolCellPhysiolです。 2010; 299(4):C750–9。
[18] Hu JJ、Liu X、Xia S、他。 FDA承認のジスルフィラムは、ガスデルミンDの細孔形成をブロックすることにより、ピロトーシスを抑制します。 NatImmunol。 2020; 21(7):736–745。
[19] Zhang Y、Zhang R、Han X.ジスルフィラムは、ガスデルミンDの切断とピロトーシスを阻害することにより、ラット片側尿管閉塞モデルの炎症と線維症を阻害します。 InflammRes。 2021; 70(5):543–552。
[20] Yu K、Li D、Xu F、他。 糖尿病性腎症の新しい免疫バイオマーカーとしてのIDO1とその免疫細胞浸潤との相関。 IntImmunopharmacol。 2021; 94:107446。
[21] van Furth R、コーンZA。 単核食細胞の起源と動態。 JExpMed。 1968; 128(3):415–435。
[22] Nelson PJ、Rees AJ、Griffin MD、他。 腎臓の単核食細胞系。 J Am Soc Nephrol 2012; 23(2):194–203。
[23] Chow F、Ozols E、Nikolic-Paterson DJ、他。 マウス2型糖尿病性腎症のマクロファージ:糖尿病状態および進行性腎障害との相関。 KidneyInt。 2004; 65(1):116–128。
[24] Chow FY、Nikolic-Paterson DJ、Ma FY、他。 単球化学誘引物質タンパク質-1-によって誘発される組織の炎症は、腎障害の発症に重要ですが、肥満のdb/dbマウスの2型糖尿病には重要ではありません。 糖尿病。 2007; 50(2):471–480。
[25] Klessens CQF、Zandbergen M、Wolterbeek R、他。 2型糖尿病患者の糖尿病性腎症におけるマクロファージ。 ネフロールダイヤル移植。 2017; 32(8):1322–1329。
[26] Rousselle A、Kettritz R、Schreiber A.単球は、抗ミエロペルオキシダーゼ抗体誘発性糸球体腎炎の三日月形成を促進します。 JPatholです。1908-1915;187(9):2017.
[27] Castellano G、Trouw LA、Fiore N、他。 浸潤性樹状細胞は、マウスおよびヒトのループス腎炎におけるC1qの局所合成に寄与します。 MolImmunol。 2010; 47(11–12):2129–2137。
[28] Tucci M、Quatraro C、Lombardi L、他。 活動性ループス腎炎における形質細胞様樹状細胞の糸球体蓄積:インターロイキンの役割-18。 関節炎リューム。 2008; 58(1):251–262。
[29] Evers BD、Engel DR、Bohner AM、他。 CD103と腎臓樹状細胞は、IL -10-制御性T細胞を産生することにより、三日月形のGNから保護します。 J Am Soc Nephrol 2016; 27(11):3368–3382。
[30] Brahler S、Zinselmeyer BH、Raju S、他。 実験的GNにおける樹状細胞サブセットの反対の役割。 J Am Soc Nephrol 2018; 29(1):138–154。
[31] Xiao X、Ma B、Dong B、他。 NODマウスの糖尿病性腎症の初期段階における細胞性および体液性免疫応答。 J自己免疫。 2009; 32(2):85–93。
[32] Soos TJ、Sims TN、Barisoni L、他。 CX3CR1と間質樹状細胞は、腎臓全体に隣接するネットワークを形成します。 KidneyInt。 2006; 70(3):591–596。
[33]KrugerT.健康なネズミの腎臓および実験的糸球体腎炎における樹状細胞の同定および機能的特徴づけ。 J Am Soc Nephrol 2004; 15(3):613–621。
[34] Cheng M、Gu X、HerreraGA。 急性尿細管間質性腎炎患者の腎生検における樹状細胞。 ハム病理学。 2016; 54:113–120。
[35] Cheng M、Gu X、Turbat-Herrera EA、他。 尿細管損傷と樹状細胞の活性化は、軽鎖関連急性尿細管間質性腎炎の不可欠な要素です。 Arch PatholLabMed。 2019; 143(10):1212–1224。
[36] Mensah-Brown EP、Obineche EN、Galadari S、他。 ラットにおけるストレプトゾトシン誘発糖尿病性腎症:炎症性サイトカインの役割。 サイトカイン。 2005; 31(3):180–190。
[37] Moon JY、Jeong KH、Lee TW、他。 糖尿病性腎症におけるT細胞の異常な動員と活性化。 Jネフロールです。 2012; 35(2):164–174。
[38] Liu BC、Tang TT、Lv LL、他。 尿細管損傷:慢性腎臓病への原動力。 KidneyInt。 218; 93(3):568–579。
[39]LinkermannA.急性腎障害および移植における非アポトーシス細胞死。 KidneyInt。 2016; 89(1):46–57。 6672 Y. JIAETAL。
[40] Linkermann A、Skouta R、Himmerkus N、他。 同期した尿細管細胞死はフェロトーシスを伴います。 Proc Natl Acad Sci US A. 2014; 111(47):16836–16841。
[41] Martin-Sanchez D、Ruiz-Andres O、Poveda J、etal。 腎毒性葉酸誘発性AKIでは、ネクロトーシスではなくフェロトーシスが重要です。 J Am Soc Nephrol 2017; 28(1):218–229。
[42] Mulay SR、Linkermann A、AndersHJ。 腎臓病における壊死性炎症。 J Am Soc Nephrol 2016; 27(1):27–39。
[43] Cookson BT、BrennanMA。 炎症誘発性プログラム細胞死。 トレンド微生物。 2001; 9(3):113–114。
[44] Zheng Z、LiG.炎症性疾患および癌におけるピロトーシスのメカニズムと治療的調節。 Int JMolSci。 2020; 21(4):1456。
[45] Wang S、Yuan YH、Chen NH、他。 NLRP3インフラマソーム/ピロトーシス活性化のメカニズムとパーキンソン病におけるそれらの役割。 IntImmunopharmacol。 2019; 67:458–464。
[46] Hoseini Z、Sepahvand F、Rashidi B、他。 NLRP3インフラマソーム:その調節とアテローム性動脈硬化症への関与。 J細胞生理学。 2018; 233(3):2116–2132。
[47] Vande Walle L、Van Opdenbosch N、Jacques P、他。 A20によるNLRP3インフラマソームの負の調節は関節炎から保護します。 自然。 2014; 512(7512):69–73。
[48]WuthrichRP。 マウスループス腎炎における血管細胞接着分子-1(VCAM -1)の発現。 KidneyInt。 1992; 42(4):903–914。
[49] Rubio-Guerra AF、Vargas-Robles H、Lozano Nuevo JJ、他。 タイプ-2糖尿病性高血圧患者における循環接着分子レベルとアルブミン尿の間の相関。 腎臓血液プレス解像度。 2009; 32(2):106–109。
[50] Sun L、Sun C、Zhou S、他。 タムスロシンは、糸球体内皮細胞の高グルコース誘発性損傷を軽減します。 バイオエンジニアリング。 2021; 12(1):5184–5194。
[51] Lin Y、Kirby JA、Browell DA、他。 腎同種移植片拒絶反応:尿細管上皮細胞におけるVCAM-1の発現と機能。 ClinExpImmunol。 1993; 92(1):145–151。

