ブロイラー鶏におけるオリーブ植物水からのフェノール化合物の使用:腸内細菌叢および胸肉の貯蔵寿命への影響パート3
Mar 12, 2022
お問い合わせくださいoscar.xiao@wecistanche.com詳細については
2.7。脂質の酸化
二次(TBAR)および一次(D232およびD270)の測定を通じて脂質酸化を研究した酸化化合物(表7)。 3つの実験グループ間で有意差は認められませんでしたが、L1およびL 0グループの鶏と比較してL2グループの鶏のTBAR値がわずかに増加したことは注目に値しますが、D232反対の傾向を示した。 これらの2つの分析指標は有意に相関していました(TBAR対D232 r =-0。5、p<0.001 and="" tbars="" vs.="" d270r=""><0.05). the="" cooking="" treatment="" caused="" decreases="" in="" the="" primary="" oxidation="" products=""><0.01), which="" were="" followed="" by="" increases="" in="" the="" secondary="" ones="" (p=""><0.001). no="" interactions="" between="" diet="" and="" cooking="" were="" observed.="" on="" the="" contrary,="" [31]and="" [45]="" observed="" a="" significant="" reduction="" in="" tbars="" in="" the="" breasts="" from="" chickens="" whose="" diets="" were="" supplemented="" with="" either="" olive="" cake="" or="" omww.="" similarly,="" [46]="" observed="" a="" reduction="" in="" tbars="" in="" the="" quadriceps="" femoris="" of="" chickens="" whose="" diets="" were="" enriched="" with="" omww="" permeate="" and="" the="">

桶他 [16]異なる量のオリーブ葉抽出物(5、10、および15 mL /リットル)をAbor acre株ブロイラーに供給される飲料水に加え、マロンジアルデヒド(MDA)の血中濃度の低下に対する有意な効果を観察しました。 イブラヒムら。 [42]は、発酵または酵素発酵した乾燥オリーブ搾りかすのレベルを上げて飼料を加えることによって得られた鶏の胸肉のMDA濃度の有意な減少を観察しました。 他の研究とは異なり、現在の研究では、筋肉組織の筋肉脂肪の酸化に対する保護効果は観察されませんでした。 研究間のばらつきと差異を生み出す多くの要因があります。 動物の品種と肥育期間の長さは別として、食事の栄養成分、飼料摂取量、環境温度、その他のストレスの多い条件などの他の要因は、比較が難しいことが多い非常に異なる結果につながる可能性があります。 活性化合物の濃度と追加の物質の存在のために、食事がフェノールで強化されているマトリックスのタイプ(オリーブケーキ、オリーブ搾りかす、オリーブ葉抽出物、植物水抽出物、ほんの数例)は長続きしません同じマトリックスに相乗作用または保護作用が存在する場合、invivoおよび屠殺後の肉組織の両方で抗酸化作用に大きな影響を与える可能性があります[47]。 新鮮な肉や肉製品に抗酸化添加物を統合することによる潜在的な健康上の利点は、常に証明されているわけではありません[48]。 それどころか、多くの一次および二次脂質およびタンパク質酸化化合物、ヒドロペルオキシド、エポキシド、4-ヒドロキシノネナール、 マロンアルデヒド潜在的な発がん性物質として認識されているか、カルボニル化合物の場合のように細胞のシグナル伝達に影響を与える可能性があります[49]。 新鮮な肉の場合、動物の配給によって抗酸化能を高める可能性は、特に合成物質ではなく天然物質の使用において、非常に示唆に富む見通しです。 実際、技術が抗酸化能を高めるための介入のさまざまな可能性を提供する肉ベースの製品とは異なり、新鮮な肉では、動物の食事による介入の唯一の代替手段は、製品の表面を対象とした治療ですが、施行されている法律と一致している。 本研究の胸肉で測定されたフェノールの残留量は、直接的な健康上の利益を引き起こす可能性は低いですが、間接的には可能です。 たとえば、肉の調理は、組織の抗酸化防御の正味の損失を引き起こします。したがって、次の場合のように、熱処理後もまだ活性である化合物による肉組織の濃縮が行われます。フェノールは、製品自体の貯蔵寿命と安全性の向上という観点から、アプリケーションにとって非常に興味深いものです。 CPCを使用した摂食試験の結果として、ビデオ内またはビデオ外の効果が観察されなかった理由は、特に間の相互作用に関して、さらに実験的な調査に値します。食事性ポリフェノールそしてそれがフェノールの潜在的な生化学的効果のかなりの部分を利用する鶏の腸内細菌叢[9,10]。

3.材料と方法3.1。 実験施設
この試験は、6か月のダウンタイムの後、パドヴァ大学(レニャーロ、パドヴァ、イタリア)の実験農場の鶏舎で実施されました。 鶏舎には、冷却システム、強制換気、放射加熱、および制御された照明システムが装備されていました。 合計12本のワイヤーネットペン(2.5×2.4m; 6m2)を使用し、それぞれに5つのニップルドリンカー(距離:20cm)と手動で飼料を分配するための円形フィーダー(直径:30cm)を装備しました。 各ペンの床は、木の削りくず(深さ5 cm、2.5 kg / m)で覆われたコンクリートの床でした。
鶏が鶏舎に到着してから最初の2日間は、24時間/日で照明が提供されました。 その後、18L:6Dの日長が達成されるまで、光の時間数が徐々に減少し、その後、12日齢以降維持されました。

Cistancheは免疫力を向上させることができます
3.2。 動物、実験グループ、およびinvivo記録
この研究は、パドバ大学の動物実験倫理委員会(Organismo per la Protezione del Benessere Animale; OPBA)によって承認されました(プロジェクト17/2016; 2016年5月10日のNo154392)。すべての動物は原則に従って取り扱われました。実験およびその他の科学的目的で使用される動物の保護に関する指令2010/63/EU[50]の。 動物の取り扱いに関与した研究者は、動物の専門家(PhDまたは動物科学の修士号)および/または獣医のいずれかでした。
合計144 1-日齢のヒナ(ロス308)が、理事会規則(EC)no.1 / 2005 [51]に準拠して、商用トラックで大学の実験施設に配送されました。 すべてのヒヨコは、孵化場でマレック病、伝染性気管支炎、ニューカッスル病の予防接種を受けていました。 雛は到着日に個別に体重を測定し、脚のマークで識別し、12羽の囲い(1羽あたり12羽、1羽あたり10羽/m²)にランダムに割り当てました。),その後、週に1回体重を測定して、商業的に屠殺されるまでの生体重を測定しました。 試験中、ペンの飼料消費量を毎日測定した。 試験中、3つの市販の食餌を砕いた形で投与しました(Martini SpA Longiano、Forli-Cesena、イタリア):0から23日までの食餌P1、24から37日までの食餌P2、および38日からまでの食餌P3 48日で屠殺(分析データの補足資料、表S1を参照)。 粗フェノール濃縮物(CPC)は、[12]に記載されているように得られました。簡単に説明すると、OVWは、ペクチナーゼおよびヘミセルロース活性を持つ酵素を使用して処理され、精密ろ過、限外ろ過、および逆浸透にかけられました。 i)L 0対照飼料(P3)、(ii)L1対照飼料とCPC(理論上の総フェノールとして220 mg / kg飼料)、(i)L2対照飼料とCPC(理論として440 mg / kg飼料)総フェノール)。 CPCおよび飼料の個々のフェノール化合物の実際の含有量を表S2に報告しました。 各食餌は4つの囲いで複製されました(初期の生体重と変動性が均一)。 CPCは、生後24日(d)から48日での商業的屠殺まで供給されました(CPCのフェノール組成については補足資料を参照)。 試験中、すべての動物に自由に餌を与え、補足食を毎週用意した。
腸内微生物群集の構成を決定するために、23、34、および44日齢で総排泄腔スワブを収集し(4匹/ペン)、合計12匹の動物(各食餌で4匹)を3回テストしました(36スワブ)。合計で収集されたサンプル)。
3.3。 商業的屠殺、および死骸と肉の品質記録
48日齢で、飼料と水を抜いた後(それぞれ、7時間と2時間)、すべての鶏を商業用食肉処理場で屠殺しました。 鶏は、クレートする前に個別に計量されました。 囲いからのすべての鶏は輸送ケージ(高さ、62.5cm×16 0cm×25.0cm;床面積)に積み込まれました。, 1 m²)。 実験施設から商業食肉処理場への積み込みと輸送、および食肉処理前の飼育には約3時間かかりました。 鶏肉は、商業食肉処理場の標準的な慣行に従って屠殺されました。 死骸は2度で2時間冷蔵した後に回収され、と畜場のドレッシング率を測定するために個別に計量されました[52]。
屠殺の24時間後、胸筋から分離された大胸筋を得るために死骸を解剖しました[53]。
試験中、死亡率のために17.4パーセント(25羽の鶏)の損失が記録されました。 119の死骸のうち、72は貯蔵寿命期間中に微生物学的分析に割り当てられ(セクション2.4は、培養依存および非依存の方法による乳房微生物相組成の確立を説明している)、残りの47は凍結された(-40)。度)、その後、生肉および調理済み肉の近似組成および脂質酸化速度の評価に使用されます(3.5項)。

3.4。貯蔵寿命の評価
3.4.1。パッケージ化された鶏の胸肉の準備
Pの主要な筋肉は、12μmの厚さのPVCフィルムで包まれた低密度ポリエチレントレイに個別にパッケージ化されました。(ワイゲル,KOEX412,Gruppo Fabbri,ヴィニョーラ,モデナ,イタリア)および冷蔵キャビネット(Majolo "Plus 1 00 Seasoning Controller、Majolo、Cadoneghe、Padova、Italy)に4±1度で保管。光への露出は8:00から修正されました。 36 W蛍光灯を使用して20:00まで[54]。保管設定は、販売中の冷蔵条件を模倣することを目的として設計されました。パッケージは、から24、72、120、180、216、および264時間にランダムにサンプリングされました。屠殺日
3.4.2。 官能分析
新鮮な乳房の官能評価は、デメリット3-ポイントスコアリングシステム(1=許容できない、2=許容できる、3=良質)を使用して[37]に従って実行されました。 合成感覚指数(SI)は[(2×臭気スコア+2×色スコア+1×テクスチャスコア)/ 5]として計算され、1.8のスコアが甘やかされて育ったサンプルを定義するためのしきい値として機能します。 官能分析は、訓練を受けた8人のパネリストによって行われました。
3.4.3。貯蔵寿命期間中の胸肉の微生物学的分析
微生物学的分析は、[38]に記載されている手順に従って実施されました。 大胸筋(長さ約2cm×深さ1cm×幅2cm)を各乳房に沿って無菌的に切除し、乳房あたり25個の代表的なサンプルを得た。 サンプルをストマッカーバッグ内で225mLの緩衝ペプトン水と混合し、適切に希釈した後に分析しました。 DNA抽出のために、各ホモジネート1mLを2mLエッペンドルフチューブに収集し、13,500×gで1分間遠心分離しました(エッペンドルフ遠心分離機5425、ハンブルグ、ドイツ)。 次に、上澄みを廃棄し、ペレットを-80度で凍結させた。 いくつかの微生物標的を調査して、貯蔵寿命期間中の微生物集団の動態を次のように説明しました:総生菌数(TVC)と総精神栄養数(TPC)をプレートカウント寒天培地(Biokar Diagnostics、Beauvais、France)で評価しました。 、およびプレートを30度で72時間または4度で10日間インキュベートした。 腸内細菌科は、バイオレットレッド胆汁グルコース寒天培地(Biokar Diagnostics、Beauvais、フランス)を用いて37度で24時間数えた。 乳酸菌(LAB)は、De Man、Rogosa、およびSharpe Agar(Biokar Diagnostics、Beauvais、France)で、嫌気性条件下、30度で48時間分析されました。 緑膿菌属。 カウントは、セトリミド、フシジン、およびセファロリジンを補充したシュードモナス寒天ベースで、25度で48時間評価した(Oxoid Ltd.、Basingstoke、Hampshire、UK)。 H2S産生細菌(推定Shewanella spp。)のカウントは、鉄寒天培地(Lyngby、Laboratorios Conda、Torrejon de Ardoz、スペイン)で25度で48時間行いました。 結果はlog10CFU/g肉として報告されます。
3.4.4。pHとドリップロス
特定の電極(メトラー・トレド、ミラノ、イタリア)を備えたpHメーター(Portamess 910、Knick、ベルリン、ドイツ)を使用して、大胸筋の腹側に3重に挿入してpH値を測定しました。 ドリップロスは、バッグ法を使用して[55]によって提示された方法に従って評価されました。 背側乳房の表面から切り取った約2.5cmのスライスをポリ袋に挿入し、2±1℃で一晩懸濁させた。ドリップロス(パーセント)は次の式で計算した:[(初期重量-最終重量)/初期重量]。
3.4.5。 食事中および胸筋中のフェノール濃度
フェノールの抽出は、5 0 mLのメタノール/水(20mg / Lのブチル化ヒドロキシトルエン(BHT)を含む80/20(o / o)溶液)と混合した5gの細かく刻んだ食事サンプルで行いました。ロッドディスパーサー(IKA、T50 Ultra-Turrax、Werke、Staufen、ドイツ)を使用して7000 rpmで1分間ホモジナイズし、9327×gで10分間遠心分離し、上清を回収しました。この手順を2回繰り返し、抽出物を回収しました。次に、ロータリーエバポレーター(Buchi Rotavapor、R -210、スイス)で最終容量が20mLになるまで濃縮しました。SPEBondElutJr-C18,1 gカートリッジ(Agilent Technologies、サンタクララ、カリフォルニア州、米国) )、事前に10mLのメタノールと10mLの水で活性化し、1mLの水性抽出物をロードしました。溶出は50mLのメタノールで行いました。真空下で溶媒を除去した後、フェノール抽出物を1mLの溶液に溶解しました。メタノール/水(50:50 v / v)で構成され、ポリビニリデンフルオリド(PVDF)遠心フィルター(0.2 mm)でろ過されます。 抽出物のフェノール化合物の定性および定量分析は、[31]に従って実施されました。
HPLC(Mod。1100 Agilent Technologies、Santa Clara、CA、USA)、C18カラム(Spherisorb ODS -1(250mm×4.6mm)5 um粒子サイズ、Waters SpA(ミラノ、イタリア)提供)フェノール化合物は、280 nmに設定されたDADを使用して検出されました。ポリフェノールの定量は、各化合物の単一のキャリブレーション曲線を使用して決定され、結果はmg kg -1として表されます。ヒドロキシチロソル(3、{{ 10}} DHPEA)はCabru SpA(ミラノ、イタリア)から入手し、チロソルp-HPEAはMerck Life Science Srl(ミラノ、イタリア)から購入し、verbascosideはExtrasynthese(Genay、フランス)から入手しました。デカルボキシメチルオルヨーロッパインアグリコン(3、4- DHPEA-EDA)は、[56]から報告された手順に従ってバージンオリーブオイルから抽出されました。
合計10グラムの肉を50mLのメタノールと水と混合しました(80/20,o/ø)ギ酸{{0}}。2パーセントと20mg/LのBHTを含みます。 ロッドディスパーサー(IKA、T50 Ultra-Turrax、Werke、シュタウフェン、ドイツ)を使用して溶液を7000 rpmで1分間ホモジナイズし、4146×gで10分間遠心分離し、上清を回収しました。 操作を2回繰り返し、抽出物の2つのアリコートを収集し、メタノールをロータリーエバポレーター(Buchi Rotavapor、R -210、スイス)で除去しました。 20mLの水性抽出物をSPEBondElut HF Mega BE-C18,5gカートリッジ(Agilent Technologies、米国カリフォルニア州サンタクララ)にロードし、事前に20mLのメタノールと20mLの水で活性化しました。 溶出は50mLのメタノールで行いました。 真空下で溶媒を除去した後、フェノール抽出物をメタノール/水からなる溶液0.5mlで回収した。(50∶50 o/ø)ポリフッ化ビニリデンでろ過します(PVDF)シリンジフィルター(0 .2mm)。 フェノール抽出物のHPLC分析は、上記と同じ装置を使用して[56]に従って実施しました。 ヒドロキシチロソールは、280nmの励起波長と313nmの発光で動作する蛍光検出器(FLD)を使用して検出されました。 ヒドロキシチロソールの定量は、検量線を使用して行われ、結果はug/kgとして表されます。

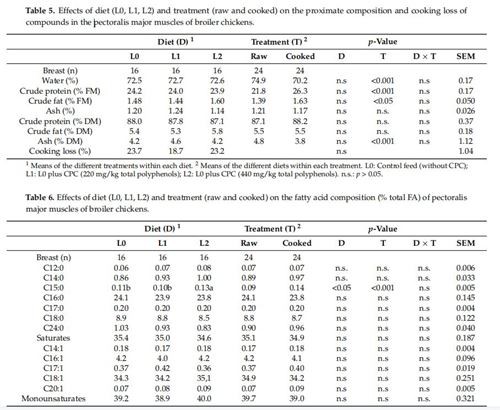
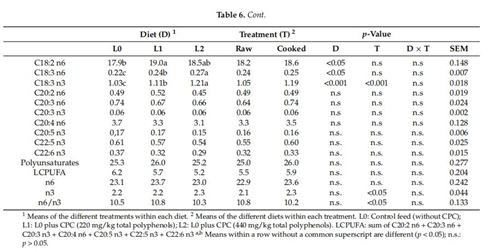
3.5。 近似組成、調理損失、および酪酸分析
生のサンプル(右側のP. major)と調理済みのサンプル(左側のP. maijor)の両方で、近似組成、脂肪酸プロファイル、および酸化安定性を評価しました。 解凍後、次の変更を加えて[53]に従って調理損失を評価しました。各胸の左半分の重さを量り、真空パックし、80度の水浴で45分間調理しました。 その後、乳房を4度までブラスト冷却し、冷蔵庫(4度)に72時間保管した後、開梱し、再度計量して、調理損失を[(生肉重量-調理肉重量)/生肉重量として計算しました。 ]×100)。 生および調理済みの筋肉を細かく粉砕し(2500rpm×10秒、Retsch、デュッセルドルフ、ドイツ)、水分、粗タンパク質、および灰分[57]分析を行い、粗脂肪含有量は提示された方法を使用して決定しました。 [58]による。 簡単に説明すると、200 mLのジクロロメタン/メタノール1:1混合物を5gのサンプルに加え、11、000 / minで1分間ホモジナイズし(Ultraturrax T25 Basic、Ika Werke。Staufen、ドイツ)、オーブン(PIDシステム、M 120- VF、MPN機器、Bernaggio、MB、イタリア)で20分間60℃。 続いて、さらに100 mLのジクロロメタンを添加し、ホモジナイズ(11、000 / minで1分間)した後、サンプルをろ過し(急速濾紙)、100mLのKCl1Mを透過液に添加しました。 1000×gで4度で30分間遠心分離(AvantiJ-E、Beckman Coulter、Brea、CA、USA)した後、上澄みを排出し、有機抽出物を無水硫酸ナトリウムで濾過した。 アリコート(約10 g)を体脂肪率の重量測定に使用し、残りを蒸留し(Rotavapor "R -210、Büchi、エッセン、ドイツ)、無水脂肪をさらに分析するために使用しました。脂肪酸メチルエステル(FAME)は、0.015 gの無水脂肪をスクリューキャップ付きのガラス管に量り取り[39]、1mLの3Mメタノール性HCl(Sigma-Aldrich、St. Louis、MO、USA)で可溶化して調製しました。次に、60度で2時間インキュベートしました。次に、1 mLの脱イオン水を加え、,混合後,FAMEは1mLのn-ヘキサンで回収されました。 FAME(1 μL)水素炎イオン化検出器(25 0度に設定)とスプリットスプリットレスインジェクター(に設定)を備えたガスクロマトグラフ(Shimadzu Italia Srl、モデル2 0 14、ミラノ、イタリア)で分析しました。 280度)。 キャピラリーカラム(Supelco SP -2560; 100m×0.25mm×0.2um)を保持するサーマルチャンバーを60度で8分間保持しました。 次に、温度を10度/分の速度で1分間120度に上げ、次に2.5℃/分の速度で120度から240度に上げた。 最終等温線は240度で20分間維持されました。 酪酸は、外部標準混合物(37 Component FAME Mix、Supelco、ドイツ)を使用して同定されました。 分析は重複して行われました。
3.6。脂質の酸化
一次酸化化合物は、Council Reg.EU / 2 015/1833[59]の付録に示されている方法の修正版を使用した紫外線フィールドでの分光光度分析によって共役ジエンとして決定されました。 簡単に説明すると、0。01±0.001gの無水脂肪を10mLメスフラスコに量り取り、分光光度グレードのシクロヘキサンでマークまで溶解しました。 UV / Vis分光光度計(Mod。7800 Jasco UV / VIS、オクラホマシティ、オクラホマ州、米国)を使用して、232(共役ジエン)および270 nm(共役トリエン)での特定の吸光値を決定しました。参照。 脂質酸化の二次生成物は、[60]によって提示された方法に従って、次のように変更して決定されました。遠心管内で、5%(m / v)トリクロロ酢酸の水溶液8mLとn-ヘキサン5mLホモジナイズしたサンプル約2gに添加しました。 Ultraturraxで30秒間高速でホモジナイズした後。 サンプルを3000×g、4C(Eppendorf 5810R; Eppendorf、Hamburg、Germany)で3分間遠心分離し、上清を除去しました。 サンプルを濾紙でろ過し、ろ液2.5mlを0.02Mチオバルビツール酸水溶液2.5mLに加え、恒温槽(労働ED {{31})で95℃で35分間インキュベートしました。 }; Seelbach、バーデンヴュルテンベルク、ドイツ)。 冷却後、532nmの波長に設定された分光光度計を使用して吸光度を測定した。 データは、肉1キログラムあたりのマロンジアルデヒドのミリグラムとして表されます。 測定は、調理済みの鶏胸肉と生の鶏胸肉の両方で2回行った。
3.7。DNA抽出とNGSライブラリーの準備
DNeasy PowerSoil DNA Isolation Kit(Qiagen、Hilden、Germany)を使用してDNAを抽出しました。 胸肉のホモジネートペレットを、キットで提供されている6 00uLの溶解緩衝液で解凍しました。 総排泄腔スワブを滅菌はさみで切断し、600uLの溶解緩衝液と6uLの2-メルカプトエタノール(Sigma-Aldrich、セントルイス、ミズーリ州、米国)を含むマイクロチューブに入れました。 ボルテックスを5分間使用してチューブを十分に混合し、綿棒を取り外しました。 cloacalサンプルと胸肉ペレットの両方に、合計100mgの滅菌0.1mmビーズ(BioSpec、バートルズビル、オクラホマ州、米国)を追加し、ビーズミル(TissueLyser、Qiagen、ヒルデン、ドイツ)を使用して高速振とうステップ(30Hzで2×30秒)。 合計40μLのプロテイナーゼK(Qiagen、ヒルデン、ドイツ)を添加し、56度で90分間インキュベートしました。 このステップの後、DNeasy PowerSoil9DNAIsolationKitの製造元の指示に従いました。 DNAの濃度と純度は、分光光度計(NanoDrop ND -1000、Thermo Scientific、マサチューセッツ州ウォルサム、米国)を使用して分析しました。
2段階増幅アプローチを使用して16SDNAライブラリーを構築しました。 サンプルは20-μL反応で増幅されました,それぞれ5μLの希釈DNAで構成されています,{{0}}。4uMの各プライマー(表1)、0.25 mMデオキシヌクレオチド(dNTP)、1×Phusion HFバッファー、および1 U Phusion High-Fidelity DNAポリメラーゼ(New England BioLabs、Inc.、Ipswich 、マサチューセッツ州、米国)。 PCRは、2720サーマルサイクラー(Applied Biosystems、Foster City、CA、USA)で、95度で30秒間、60度または49℃で30秒間、72℃で45秒間の25サイクルで実施しました。 72度で7分。 サンプルごとに3回のPCR複製を実行しました。
SPRIselect Purification Kit(Beckman Coulter Life Sciences、Indianapolis、IN、USA)を使用して生成物を精製し、ビーズ精製後、1.8%アガロースゲルを使用してターゲットバンドを確認しました。 バーコードは、プラットフォーム固有のバーコードベアリングプライマーを使用した2回目のPCR分析によって導入されました。 各50-uLPCR反応には、各プライマーの0。2μMのPCR産物が含まれていました。(表1),0。3mMdNTP,1×PhusionHFbuffer,and1UPhusion高忠実度DNAポリメラーゼ。 上記のPCRプロファイルの10サイクルを実行しました。
PCR産物は、SPRIselect精製キット(Beckman Coulter Life Sciences、Indianapolis、IN、USA)を使用して精製しました。 最終精製後、Qubit 2を使用して各サンプルを定量しました。0蛍光光度計(Invitrogen、Life Technologies、モンツァ、イタリア)。 アンプリコンライブラリの品質は、Agilent 2100バイオアナライザ(Agilent Technologies、米国カリフォルニア州パロアルト)を使用してテストしました。 ライブラリは、ペアエンド300-サイクルラン(Macrogen Inc.、ソウル、韓国)を備えたIlluminaMiSeqプラットフォームを使用してシーケンスされました。
4.結論
製油所の植生水のろ過と濃縮によって得られたフェノールによる鶏の飼料の24日間の濃縮は、動物の成長、飼料要求率、または枝肉の収量の違いとは関連していませんでした。 腸内細菌叢の研究では、微生物群の交代に対する摂食時間の有意な影響が示されましたが、食事自体の影響は示されませんでした。 一方、貯蔵寿命期間中の肉の微生物相組成は、フェノールが豊富な飼料を摂取した鶏のサンプルでシュードモナスのより大きな成長を示しました。 最後に、脂質酸化プロセスの分析マーカー(TBARおよび共役ジエン)に関して、食事間で違いは観察されませんでした。 代わりに、フェノールを添加した飼料を摂取した鶏のサンプルの筋肉組織でヒドロキシチロソールが同定され、用量依存的な腸管吸収を示しました。 酸化過程は主に筋細胞の膜構造で起こるため、細胞および細胞外コンパートメントにおけるHTの分布をよりよく理解するためにさらなる研究が必要です。
この記事は、Molecules 2021、26、4307から抽出されています。https://doi.org/10.3390/molecules26144307 https://www.mdpi.com/journal/molecules
